
与传统药物洗脱支架相比,第一代生物可吸收支架(bioresorbable scaffolds ,BRSs)的支架血栓形成率较高,部分原因可能是生物可吸收聚合物的径向强度不足,因此需要更大的支架轮廓。对第一代 Absorb 生物可吸收血管支架(bioresorbable vascular scaffold,BVS)的长期疗效进行的 Meta 分析发现其超额风险期在 3 年后结束。因此,目前的关注重点是通过提高支架的抗拉强度并减少支架厚度来改善早期疗效。
本综述总结了第一代 BRS 的经验教训,更新了ABSORB BVS 和基于金属合金的 BRS 试验的长期临床结果。此外,还对亚洲生产的下一代 BRS 进行了评述【公众号只选取部分内容进行翻译,详细内容见附件原文】。

一、介绍
从40年前的球囊血管成形术到冠状动脉支架,降低了经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)后再次狭窄和目标病变血运重建(target lesion revascularization,TLR)的发生率;21世纪初从使用裸金属支架(bare metal stents ,BMS)转变为药物洗脱支架(drug-eluting stents ,DES)后,进一步改善了这种情况。尽管当前一代DES取得了很好效果,但仍然存在晚期支架内血栓形成,及其相关的高发病率和死亡率风险。生物可吸收支架(Bioresorbable Scaffolds ,BRS)能够克服金属支架的一些局限性,例如血管笼状结构导致冠状动脉血管运动的缺失。第一个BRS——IGAKI-TAMAI支架,实际上是在1999年植入的,比DES的引入早了3年。2006年,首个人体ABSORB生物可吸收血管支架(BVS,Abbott Vascular,美国)的研究被报道,该设备在2011年获得了CE标志,但由于其较高的血栓形成率而退市(2017年)。现在,仍有许多厂家采用新材料和新的结构设计开发新型BRS,以尝试克服这些不足,如下图所示。

图. 冠状动脉疾病中的BRS(BRS:生物可吸收支架;OCT:光学相干断层扫描;PLLA:聚 L-乳酸;PDLLA:聚 D、L-乳酸)
本综述不仅关注ABSORB BVS(表1)的长期结果,还将回顾为治疗冠状动脉疾病(coronary artery disease,CAD)设计的下一代BRS(表2)。
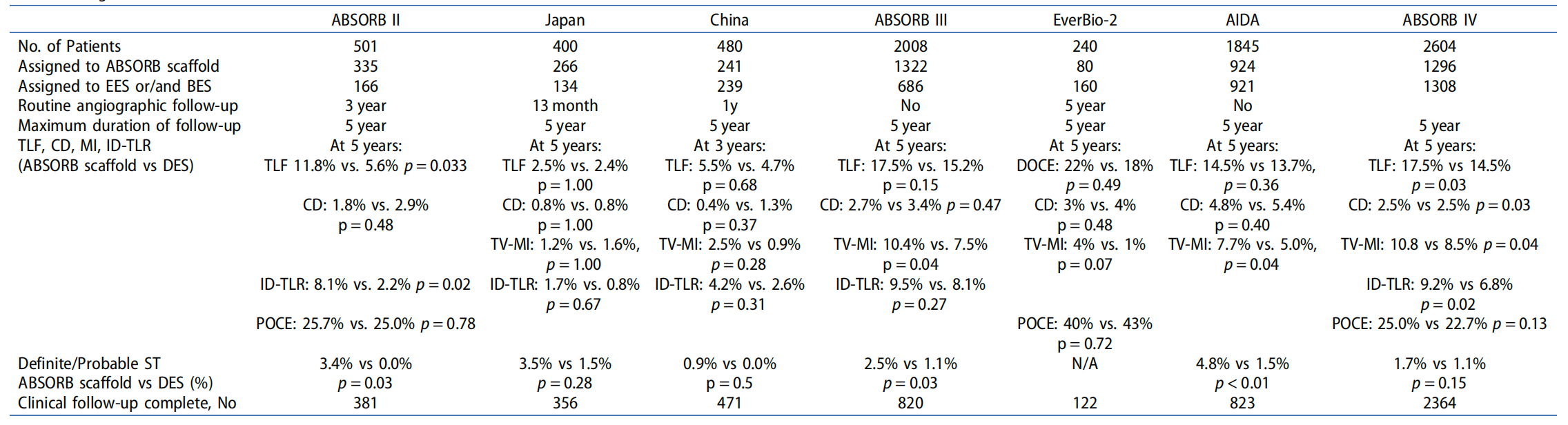
表1 Absorb BVS 随机试验的长期结果。

表2 新一代生物可吸收支架的成果
团队使用PubMed、Web of Science和Google Scholar进行了全面的文献搜索,搜索了截至2024年2月9日发表的文献,使用的关键词包括“生物可吸收支架”、“长期临床结果”、“经皮冠状动脉介入治疗”和“周围动脉疾病”,以及相关的会议记录。此外,还增加了关于生物可吸收装置在急性冠状动脉综合征患者和冠状动脉旁路移植中应用的临床试验结果的最新参考文献列表。
二、生物可吸收支架的潜在优势
生物可吸收支架与目前的金属 DES 相比具有以下几个潜在优势:
(1) 通过生物吸收去除支架血管的刚性笼状结构,有助于恢复血管的自然功能,例如血管运动、机械转导适应性剪切应力、晚期管腔扩大和血管重塑等。此外,支架能够减少永久金属支架支柱相关的侧枝闭塞并发症;
(2) 改进治疗方案,因为以前植入的DES形成的金属笼可能使重复血管重建变得具有挑战性,相比之下,使用BRS可能消除对未来血管重建的限制,允许更好地治疗复杂的多支血管疾病;
(3) 能够使用非侵入性成像,如计算机断层扫描冠状动脉造影(computed tomography coronary angiography ,CTCA)或磁共振成像(MRI)进行随访,因为金属支架会导致晕影伪影的出现。虽然非金属聚-L-乳酸(PLLA)BRS能够消除对成像的限制,但金属BRS只有在完成生物吸收后才能实现伪影的消除;
(4) BRS可以作为局部给药和基因传递的储库。由于生物可吸收的持续时间可以根据聚合物/共聚物的类型进行调整,因此有可能针对不同的再狭窄机制实现多种药物的调整洗脱(缓释);
(5) 消除患者对体内永久植入物的担忧;
(6) 可能减少潜在长期事件的发生,因为药物洗脱和支架是暂时的,只有在血管愈合之前由设备提供。没有非内皮化支柱或持久性药物聚合物等可能会触发支架血栓形成的异物;
(7) 将冠状支架的适应症扩展到功能性显著狭窄的治疗和特殊人群的治疗之外,如儿科患者。
三、下一代可吸收支架
1、新一代镁支架(DREAMS 3 G,JMDT)
BIOMAG-I试验是一项针对下一代Mg BRS(DREAMS 3 G)的FIM试验,最近的研究结果表明,与前一代DREAMS 2 G相比,DREAMS 3 G在6个月随访时显示出较低的支架内晚期管腔丢失(late lumen loss,LLL)(平均为0.21mm)。在1年随访时,支架内LLL为0.24 ± 0.36 mm,具有出色的临床安全性和有效性,其中靶病变失败(target lesion failure,TLF)和缺血驱动的靶病变血运重建(ischemia driven-TLR ,ID-TLR)分别为2.6%和2.6%;没有心脏死亡、靶血管心肌梗死(target vessel myocardial infarction ,TV-MI)或明确的/可能的支架血栓(scaffold thrombosis,ScT)发生,如下图所示。

图. BIOMAG-I试验数据。a) 光学相干断层扫描显示术后支架贴合良好,12 个月时支架已无法辨认。b) 在 BIOSOLVE-II 研究中,与 DREAMS 3 G 的前身 DREAMS 2 G 相比,障壁内晚期管腔损失(LLL)改善了 38%。c) 血管内超声的序列面积变化。有 75 名患者的血管内超声配对数据(核心实验室分析)。d). 平均管腔面积和平均支架面积几乎相同。
BIOMAG-II随机对照试验:这项试验旨在评估DREAMS 3 G设备治疗原发性冠状动脉病变患者(最多两个de novo病变)的安全性和有效性,计划于2024年开始招募患者。这项试验将比较DREAMS 3 G与当代DES(药物洗脱支架)的性能(NCT05540223)。
JMDT (JFK-01):这是一个由日本医疗器械技术公司(Kumamoto, Japan)和富士轻金属公司(Kumamoto, Japan)共同开发的镁支架,支架厚度为100微米。该设备由一种新的无稀土元素镁合金制成,具有三层防腐涂层和外层释放西罗莫司(sirolimus)。体外和临床前数据显示,这种设备在降解过程中具有改善的机械性能和可持续的径向力。目前,一项探索性的多中心、开放标签的临床研究已经开始,旨在评估JFK-01在缺血性心脏病患者中的安全性和有效性。
2、XINSORB 支架
Xinsorb BRS(山东华安生物科技有限公司,浙江杭州)是一种由PLLA 与 PDLLA 混合制成的支架,上面涂有西罗莫司(8-16 μg/mm),厚度为 160μm。在一项前瞻性多中心临床试验(SPARTA 研究:NCT04501900)中对 XINSORB 进行测试,将新发病灶患者按 1:1 的比例分配给 XINSORB 和 SES(表 2)。12 个月的随访结果显示,与 SES 相比,XINSORB 的节段内 LLL 更低(0.19 ± 0.32 mm vs. 0.31 ± 0.41 mm,p = 0.003),TLF相近;在 3 年的随访中,其TLF 和装置血栓的发生率较低,疗效和安全性相似。
3、其他支架
此外,文章就Fantom 支架【(REVA Medical,加利福尼亚州,美国),是第二代西罗莫司洗脱生物可吸收支架】、Bioheart 降解支架【(Bioheart,中国上海),由涂有洗脱西罗莫司的 PDLLA+PLLA 构成】、MeRes 100【(Meril 生命科学公司,印度古吉拉特邦瓦皮),是一种基于聚乳酸(PLLA)的西罗莫司洗脱 BRS,具有混合几何结构,可提供高径向强度、薄支柱和三轴向不透射线标记】、NeoVas【(乐普医疗,中国北京),基于 PLLA 的 BRS支架,含有涂层】等进行了详细介绍(详见原文)。
翻译文稿不免出现笔误,还请各位读者指正和谅解!如有遗漏,欢迎留言补充。
整理丨武瑾嵘
排版丨壹 万
医疗器械、新材料、人工智能;
一定技术壁垒



