
一个理想的人工心脏瓣膜应满足如下条件,如符合心脏瓣膜生物流体力学的要求、材料以及结构机械性能稳定、与肌体组织和血液的相容性好等。本篇将对高分子瓣膜材料进行概述并介绍相关公司。
机械瓣具有出色的结构耐久性,使用寿命为20-30年,但植入后易因血栓形成而产生血流动力学障碍,患者需进行终身抗凝治疗。生物瓣主要以牛心包或猪瓣膜为基础材料,现有主流产品的使用寿命约10年,植入后仅需进行3-6个月术后抗凝治疗。但机械应力、血栓形成和矿物质沉积等因素作用下发生的结构性瓣膜退化是导致生物瓣膜失效的主要原因,由此而产生的再次手术需求也限制了低龄患者的治疗效果1。
针对机械瓣和生物瓣材料的缺陷,目前的研究趋势是利用高度可调可控的天然及合成聚合物原料制备人工心脏瓣膜(AHV)。此类设计有望结合机械瓣的耐久性和生物瓣的生物相容性,通过灵活设计瓣叶的结构与组分,使AHV在力学行为和生理特性上实现原生瓣膜功能2。
一个理想的人工心脏瓣膜应满足如下条件3:
(1)符合心脏瓣膜生物流体力学的要求。即瓣膜开放阻力最小,瓣膜开放时间短,瓣口两侧无明显压力差。当瓣膜关闭时,瓣口关闭速度快、关闭严、无反流。血液通过瓣口产生的流场近似于生理血液流场,不产生涡流。
(2)材料以及结构机械性能稳定,具有较好的耐久性,在数十年的使用时间内保持瓣膜的相应功能。
(3)与肌体组织和血液的相容性好。不破坏血液成分、不凝血、不溶血、不引起机体免疫反应,以及没有噪声,不影响患者的正常生活。
(4)瓣膜的设计与制造便于外科移植手术的实施,其灭菌、保存方便,手术操作简便易行。
(5)材料易得,便于制造,价格合理,容易推广。
【原生瓣膜力学性质】
人体原生瓣膜具有复杂的组织成分和结构特性,在结构和力学方面表现出显著的各向异性。
1、结构各向异性
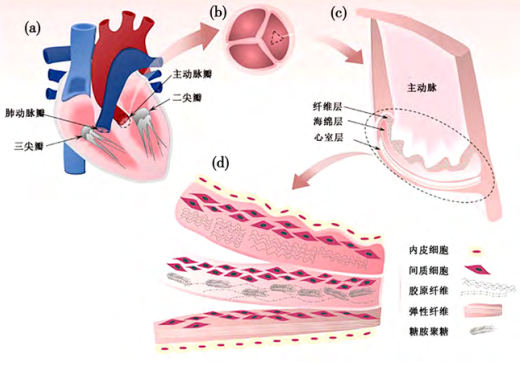
原生瓣膜的瓣叶厚度一般小于1mm,由纤维层、海绵层和心室层三层异质结构组成,整体既坚固又具备高度灵活性,可持续有效开合数10亿次。以主动脉瓣这一参与体循环的重要瓣膜为例,其瓣叶结构表现出各向异性特征。
· 面向主动脉的纤维层主要由呈周向排列的I型和III型胶原纤维组成,是心脏舒张时的主要受力层;
· 中间呈多孔凝胶状的海绵层包含大量糖胺聚糖,在多次动态循环中起缓冲作用;
· 心室层主要由呈径向排列的弹性纤维组成,为瓣叶提供充足的弹性。
主动脉瓣瓣叶各层占总厚度比例不同,纤维层一般小于45%,心室层一般小于30%。其他部位的瓣叶构成与主动脉瓣瓣叶相似,但各层在总厚度中的占比实际受物种、取样部位和测试方法等因素影响而有所差异4。由于纤维层厚度最大,承受大部分机械载荷,在构建仿生AHV材料时需要着重考虑其结构。原生瓣膜的结构赋予其合适的跨瓣压差和剪切应力,使其规律开合并被血液自然冲洗。但是,植入的机械瓣在瓣叶边缘可能产生湍流并导致血栓形成,而生物瓣通常需要一定时间才能完成组织愈合和内皮化,在此之前则易形成血栓2。
2、力学各向异性
原生瓣膜的结构使其力学性能同样表现出各向异性的特点。与大部分软组织类似,心脏瓣膜真实的力学行为表现出高度非线性的应力⁃应变关系,具有大变形、复杂的粘弹性和复杂的轴向耦合行为。这种力学行为大部分是内部结构随应变变化所致,涉及高度卷曲胶原纤维的伸直及纤维向拉伸轴的旋转,最终产生方向性的力学性能。
其中,胶原纤维网络作为瓣叶最坚固的部分,长期承载心脏搏动状态下的复杂机械负荷。单轴拉伸测试结果显示,原生主动脉瓣瓣叶的周向弹性模量为3-15 MPa,径向弹性模量为1-2 MPa,周向弹性模量和极限抗拉强度均大于径向。单轴拉伸测试虽可以显示瓣叶在两个垂直方向上存在力学性能差异(各向异性特征),但无法反映瓣叶的双轴力学行为;双轴拉伸测试能分析瓣叶每个方向响应的耦合性,更真实地模拟生理力学环境5。
【聚合物瓣膜研究历程及进展】
聚合物心脏瓣膜的概念最初是由Roe、Owsley和Boudoures在20世纪50年代提出的。1960年,一项研究报告了首次由聚氨酯材料制成的瓣膜的动物研究和临床植入反馈。但在聚氨酯材料的探索阶段,发现它们无法提供足够的耐用性6。目前聚合物瓣膜中使用的材料包括天然、合成和复合聚合物。
最早研究的材料有聚硅氧烷、聚四氟乙烯(PTFE)、聚氨酯(PU)、聚(L-乳酸-co-ε-己内酯)(PLCL)、聚(乳酸-共-乙二酸)(PLGA)、聚己内酯(PCL)、聚(乳酸-羟乙酸)(PLA)和聚(L-乳酸-羟乙酸)(PLLA)。由于生物相容性差、机械性能和钙化率高,这些聚合物材料被发现不适合用于随后的临床前测试或临床试验7。
在21世纪初,在现有的聚合物合成技术和纳米技术的帮助下,通过表面改性、材料复合和合成方法的优化获得了新型聚合物材料。这些聚合物材料在应力水平、生物相容性和降解性方面得到了改进。目前,这些新型聚合物材料包括硅聚氨酯(SiPUU)、多面体寡聚硅基喹聚碳酸酯聚氨酯(POSS-PCU)、纳米复合石墨烯聚碳酸酯聚氨酯聚合物(FGO-PCU)、聚(苯乙烯-b-异丁烯-b-苯乙烯)(SIBS)和聚(苯乙烯-b-4-乙烯基苯甲苯甲苯二烯-b-异丁烯-苯乙烯-b-4-乙烯基苯甲氧基苯甲基)(xSIBS)8。

图. 聚合物材料的开发时间表。绿色部分代表第一代聚合物材料,黄色部分代表第二代9。
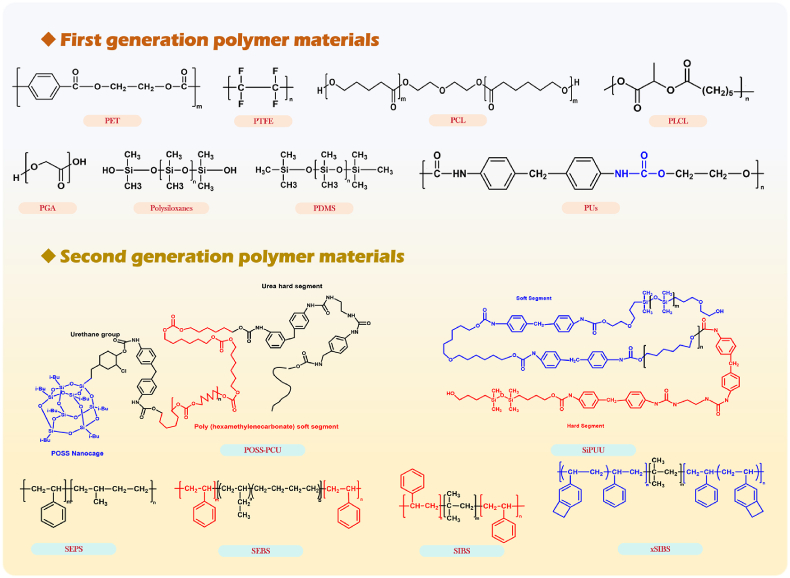
图.聚合物瓣膜材料化学分子式
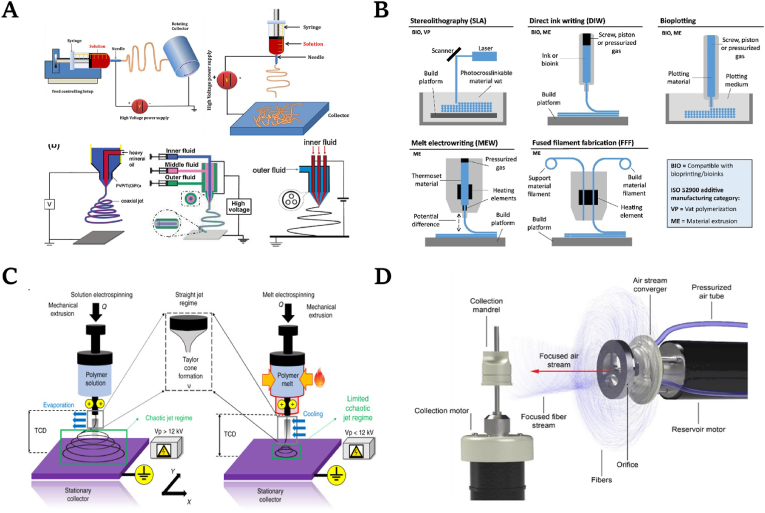
主流聚合物材料制备技术包括:静电纺丝、3D打印、熔融电纺(MEW)、聚焦旋转喷射纺(FRJS)和瓣膜构象的计算机辅助设计(CAD)(如下图所示)。
随着新型聚合物合成策略的出现,开发和设计了几种具有实际临床应用的聚合物瓣膜。Foldax® Tria™瓣膜在美国的临床试验始于2019年,共有100多例植入病例,使其成为植入最多的聚合物瓣膜。2023年,印度也进行了Tria™二尖瓣的临床试验,手术量为30例。由Junbo等人领导的团队将于2022年首次植入中国聚合物SIKELIA ™ TAVR瓣膜,已完成10多次临床试验,长期安全性和有效性数据正在等待临床随访数据的发布10。其他聚合物瓣膜(包括手术和介入)也显示出有希望的早期体外效果。
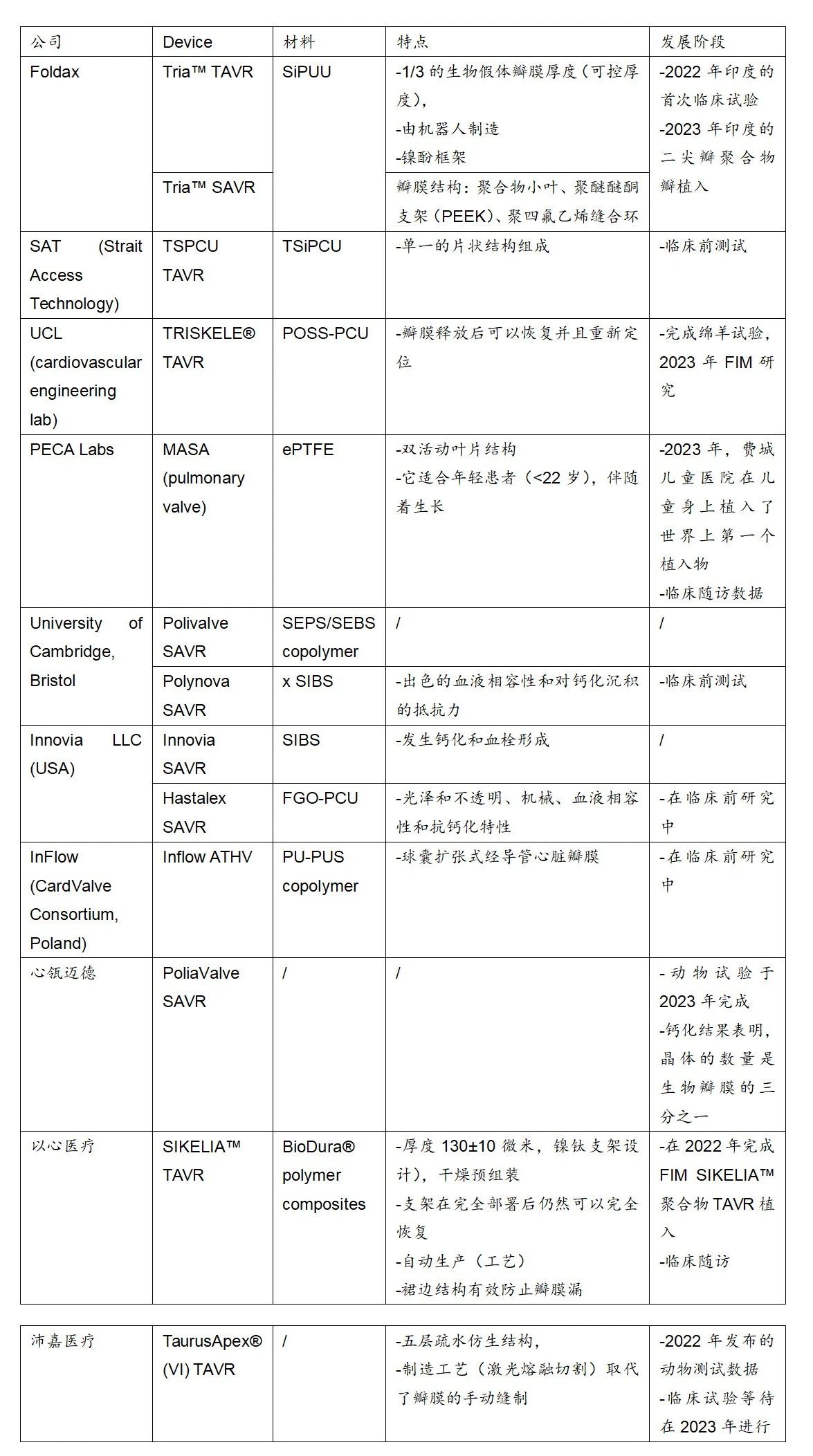

图.高分子心脏瓣膜产品(包括TAVR和SAVR)的研究现状及进展情况
【聚合物瓣膜代表公司】
1、Tria ™(Foldax®,美国)
Foldax®公司(美国)目前是全球聚合物瓣膜研发领域的先驱,Tria™心脏瓣膜平台是世界上第一个可用于主动脉、二尖瓣和三尖瓣置换的聚合物心脏瓣膜平台。它的聚合物主动脉瓣,Tria™心脏瓣,是由一种革命性的新材料——LifePolymer。选择的聚合物材料是硅基聚氨酯尿素(SiPUU),通过两步溶液聚合工艺可以合成为改性弹性聚氨酯。瓣膜厚度为生物瓣膜的1/3,Foldax® Tria™外科主动脉瓣由自膨胀镍钛合金和10毫米密封套组成。Tria™瓣膜是唯一由机器人制造的心脏瓣膜,机械化制造实现了高精度、质量和可重复性,减少了与传统瓣膜手动制造相关的不可控因素,大大提高了心脏瓣膜制造的经济性。
LifePolymer材料的测试结果表明,其生物相容性和耐用性接近人体,为进一步研究提供了坚实的基础。在加速体外疲劳测试条件下,它展示了与Edward Perimount瓣膜类似的有效开口面积和经瓣膜差压,Foldax®手术二尖瓣和经导管主动脉瓣置换装置正在进入临床阶段。根据最近的一份报告,Foldax®已于2023年在印度进入人体临床试验阶段,首批30名患者接受了Tria™手术二尖瓣心瓣11。植入一年后,患者对经瓣膜压差(TPD)、有效开口面积(EOA)和心脏功能数据的反馈显示出显著改善。
上海以心医疗自行开发的聚合物TAVR SIKELIA™在中国聚合物瓣膜研发(R&D)中处于领先地位。2022年7月,Junbo等人成功为一名80岁的患者植入了世界上第一个聚合物经导管主动脉瓣膜,将中国的瓣膜治疗研发带入了聚合物时代,并表明中国已经开始在心血管医疗设备某些领域的创新方面处于世界领先地位。2023年,世界上第一位经管聚合物TAVR患者的术后1年随访结果已经公布。
聚合物SIKELIA™ TAVR是一种自膨胀瓣,由镍钛合金与合成聚氨酯(PU)纳米复合材料组成。瓣膜材料的厚度仅为生物瓣膜的1/3,具有良好的生物相容性,聚合物表面经过设计和优化,有效减少了刺激和排斥反应,提高了瓣膜在体内的耐久性,降低了一些并发症的风险。在加工方面,铆接的金属架和叶片不需要缝合,可以实现自动化生产和标准化的质量控制,并显著降低了生产成本。创新之处在于大网孔设计和记忆合金丝铆接结构,这在一定程度上增加了瓣膜的灵活性和适应性。在实际外科手术中,对于某些复杂解剖结构和严重病变的主动脉瓣,这样的设计可以使瓣膜更好地适应并实现有效贴合,提高手术成功率。此外,聚合物SIKELIA™的设计允许轻松取出和二次定位。
TaurusApex®聚合物瓣膜是第四代独立开发的介入瓣。TaurusApex®使用五层仿生聚合物纤维编织物作为瓣膜材料,以及具有不同比例弹性体的海绵和心室层,以提供改进机械应力,同时保持类似于天然瓣膜的各向异性。TaurusApex®由激光切进行加工,减少了手动缝合的需求并提高了产量。TaurusApex®专注于解决生物假体瓣膜缺乏耐用性的问题,在这个阶段,该瓣膜在2亿次加速疲劳测试后保持稳定的血液动力学,没有明显的瓣膜损伤,展示了出色的耐用性。该瓣膜已经完成了动物研究,并准备进入临床试验。
总结:随着微创介入理念的发展,心脏瓣膜整体朝向经导管介入治疗,未来经导管治疗将占据较大比例:其中经导管主动脉置换产品相对成熟,国内厂家在经导管主动脉瓣膜置换领域占据主导地位,经导管二尖瓣治疗目前修复领域发展较快,以雅培公司为代表,逐渐打开国内市场,同样国产厂家也在今年拿下缘对缘修复产品NMPA认证,行业发展处于早期导入期,随着国产厂家进入将会快速进入成长期;对二尖瓣经导管置换产品,由于开发难度大,并且二尖瓣独特的生理解剖结构,产品大部分处于临床阶段以及早期研究阶段;最后三尖瓣瓣膜疾病整体患者基数大,但是大多数没有被重视,并且经导管三尖瓣置换与修复产品上市少,以爱德华为主要代表,未来随着三尖瓣疾病重视,将会得到长足发展。
心脏瓣膜产品材料一直是研发重点,金属,热解碳材料和生物瓣膜材料是目前产品的主流基材,但是二者都存在着暂时不能解决的缺点,并不能做到替代。现在材料研发重点转向高分子聚合物领域,产品稀缺,目前仅有一家产品进入注册临床试验,新材料是未来竞争的蓝海。
资料来源:
[1] IbrahimDM,Kakarougkas,AllamNK,Materials Today Chemistry,2017,5,11.
[2] 陈昱欣,陈诗萍,王文硕,等.仿生人工心脏瓣膜材料的研究进展[J].材料导报,2023,37(S2):548-556.
[3] 郝凤阳,苏健,孙璐,等.人工心脏瓣膜的发展[J].医疗装备,2017,30(13):186-190+193.
[4] Sacks MS, Yoganathan AP. Heart valve function: a biomechanical perspective. Philos Trans R Soc Lond B Biol Sci. 2007 Aug 29;362(1484):1369-91.
[5] Guo, F., Liu, C., Han, R. et al. Bio-inspired anisotropic polymeric heart valves exhibiting valve-like mechanical and hemodynamic behavior. Sci. China Mater. 63, 629–643 (2020).
[6] Braunwald N.S., Cooper T., Morrow A.G. Complete replacement of the mitral valve: successful clinical application of a flexible polyurethane prosthesis. J. Thorac. Cardiovasc. Surg. 1960;40:1–11.
[7] Ciolacu D.E., Nicu R., Ciolacu F. Natural polymers in heart valve tissue engineering: strategies, advances and challenges.Biomedicines. 2022;10:1095.
[8] Rezvova M.A., Klyshnikov K.Y., Gritskevich A.A., Ovcharenko E.A. Polymeric heart valves will displace mechanical and tissue heart valve s: a new era for the medical devices. Int. J. Mol. Sci. 2023;24:3963.
[9] Wang Y, Fu Y, Wang Q, Kong D, Wang Z, Liu J. Recent advancements in polymeric heart valves: From basic research to clinical trials. Mater Today Bio. 2024 Aug 10;28:101194.
[10] Ge J., Zhou D., Zhang X., Hou S., Chen S., Jin Q., Pan W., Li W., Pan C., Qian J. Preliminary implantation of a novel TAVR device with polymeric leaflets for symptomatic calcific aortic disease.JACC Case Rep. 2023;17
[11] Valk D.C.V.D., Fomina A., Uiterwijk M., Hooijmans C., Akiva A., Kluin J., Bouten C., Smits A. Calcification in pulmonary heart valve tissue engineering. JACC Basic Transl Sci. 2023;8:572–591.
[12] Ge J., Zhou D., Zhang X., Hou S., Chen S., Jin Q., Pan W., Li W., Pan C., Qian J. Preliminary implantation of a novel TAVR device with polymeric leaflets for symptomatic calcific aortic disease. JACC Case Rep. 2023;17
声明:以上根据公开资料整理。如有遗漏,欢迎留言补充。
作者:Felix
排版:壹万
转载请注明来源:和义广业创新平台
更多医械行业分析,欢迎关注和义广业创新平台公众号,回复“行研资料”,获取往期行研汇总包。旗下和义广业网(heyiguangye.com)作为医疗器械创新创业知识信息平台,提供投融资信息对接、产业化指导,并共享前沿信息、深度行研、法规标准、创新创业课程等资源。
医疗器械、新材料、人工智能;
一定技术壁垒



