
通过靶向免疫细胞本身来调节免疫细胞的功能已成为免疫疗法对抗癌症、自身免疫性疾病和传染性疾病等各种疾病的关键策略。一方面mRNA(核糖核酸)是瞬时诱导蛋白质表达的有力工具,常用于遗传操作;另一方面由于免疫细胞的抵抗机制、信号通路和细胞间的相互作用,因此转染免疫细胞既困难又复杂。本综述介绍最近开发的用于向免疫细胞递送 mRNA 的生物材料(包括脂质纳米颗粒和聚合物载体)、递送治疗面临的挑战,以及下一代材料设计的展望。(公众号只选取部分内容进行翻译解读,详细内容见附件原文)。
mRNA、免疫系统、mRNA递送、疫苗、生物材料、免疫疗法

mRNA 是指导细胞内蛋白质合成的模板,可用于指导细胞生产特定的蛋白质。通过将合成的 mRNA 引入人体可引导细胞产生所需的蛋白质,并触发靶向免疫反应,释放免疫系统的潜能。然而,由于裸露的mRNA 分子无法稳定的在适当的时间内输送到适当的细胞和组织中,因此,其作为药物使用受到很大限制。在这种情况下,mRNA递送材料的研发就显得尤为重要,目前研究的递送材料包括脂质纳米颗粒和聚合物,它们可提供保护载体、提高细胞吸收率并优化治疗的效果。
在这篇综述中,旨在概述利用脂质和聚合物纳米颗粒递送免疫细胞的最新突破。鉴于免疫细胞在免疫功能和整体健康中的关键作用,了解免疫细胞在全身的分布至关重要,这种分布形成了一个复杂的系统,其中不同的免疫细胞发挥着不同的作用。如图所示,淋巴系统中的免疫细胞浓度最高,包括淋巴结、脾脏、胸腺、扁桃体和骨髓,然而,在感染、癌症或特定条件下,这种分布会发生显著变化。掌握免疫细胞群的异质性以及免疫组织和器官错综复杂的组织结构是一项重大挑战,对于开发能够在体内外选择性地靶向这些细胞类型的生物材料也是不可或缺的。

图. (A) 造血的各个阶段 (B)人体各部位免疫细胞分布示意图 (C) 人体内不同免疫细胞的相对丰度图。
脂质纳米颗粒(Lipid nanoparticles,LNPs)是一种很有前景的基因治疗递送技术,它可以克服生理障碍,且没有病毒递送的可能存在的潜在风险【辉瑞和Moderna已成功利用 mRNA 脂质纳米粒开发出 COVID-19 疫苗,此外Alnylam公司的siRNA LNP 药物Onpattro也成功治疗遗传性跨甲状腺素介导的淀粉样变性病】。
LNP 由四种不同的脂质成分组合而成,其中包括一种带有叔胺或季胺的可离子化脂质或阳离子脂质,可与 mRNA 相互作用;一种齐聚物脂质,有助于形成双分子层结构;胆固醇作为 LNP 脂质双分子层的间隔物,可稳定 LNP;以及一种聚乙二醇 (PEG) 脂质,可减少蛋白质吸收并增强胶体稳定性,如图所示。
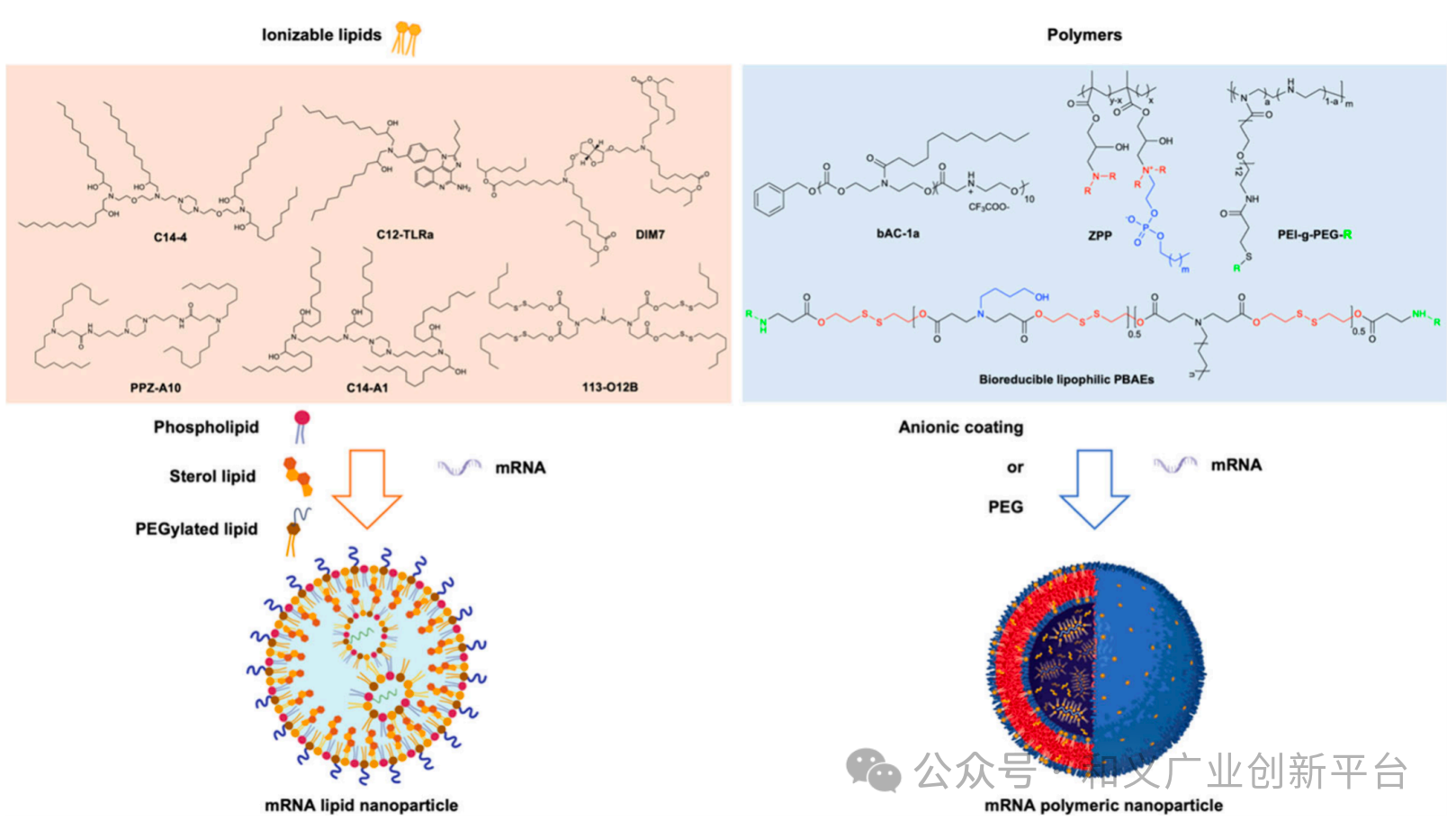
图. 使用脂质和聚合物纳米颗粒向免疫细胞传递 mRNA
用脂质纳米颗粒递送的药物在给药后,递送体(LNP)会与血液蛋白相互作用,形成一层称为 "电晕 "的涂层,这种涂层被认为能改变其表面性质和理化特性,有助于其器官靶向和细胞内吞。尽管已知 LNP 递送系统能有效地进入包括淋巴细胞在内的各种细胞类型,而且细胞毒性极低,但如何将 mRNA LNP 有效地递送到免疫细胞仍是一项重大挑战。免疫细胞是人体的守护者,很难进行转染,在免疫疗法和细胞疗法中往往需要进行体外改造,然后再输回患者体内,如美国食品及药物管理局(FDA)批准用于嵌合抗原受体CAR-T 细胞疗法等治疗的主要方法就是电穿孔法。
近期有团队研究在向体内免疫细胞输送 mRNA 以进行免疫调节方面取得了重大进展,其原理是使用含有免疫细胞受体激动剂的可电离脂质纳米颗粒,使其与免疫细胞密切配合,引起随后的内吞作用。Han 等人开发了一种新型佐剂类脂基 LNP 系统,其将佐剂作为一种结构成分,增强了系统的选择性、转染性和佐剂性,如下图所示。这种脂质系统C12-TLRa通过Toll样受体7/8(TLR7/8)激动剂1的胺基与C12环氧化物之间的精确开环反应合成的,经过优化后,该系统将这种类脂质与由三胺前体与 C12 脂链融合而成的可离子化脂质 C12-113 结合在一起,从而提高了 mRNA 的传递效率。实验结果表明,树突状细胞的转染效率明显提高,且呈剂量依赖性;C12-TLRa的加入大大增强了LNPs的佐剂性,从而显著提高了皮下注射的mRNA递送效率。
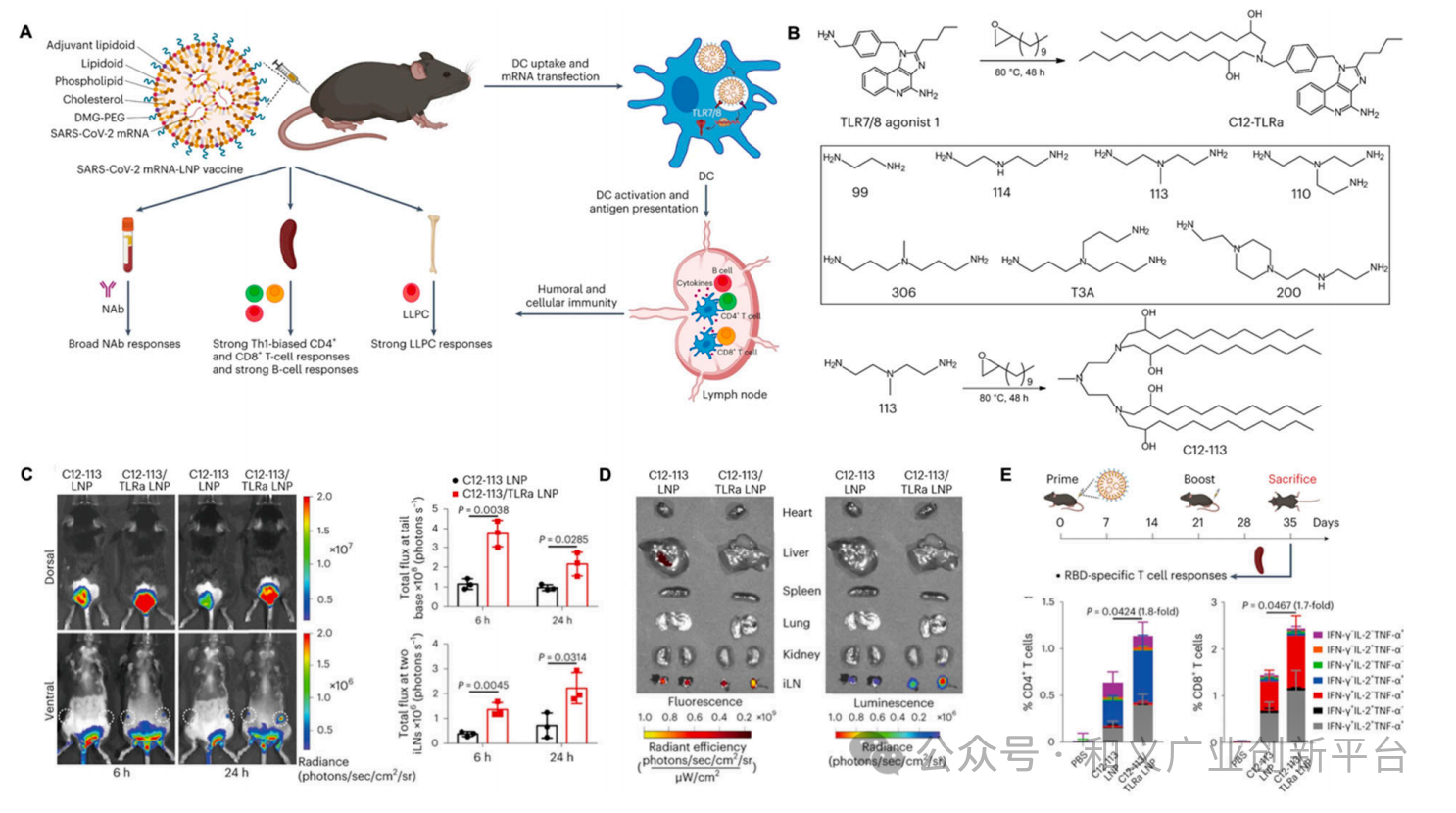
图. 基于类脂佐剂的脂质纳米粒子系统。(A) 佐剂类脂疫苗增强适应性免疫的作用机制图解。(B) 佐剂类脂质 C12-TLRa 通过 TLR7/8 激动剂 1 和环氧化物 C12 之间的开环反应形成,同时合成多胺衍生类脂质 C12-113。(C)用 mLuc 负载的 LNPs 处理后 6 小时和 24 小时进行的生物发光成像,图像显示了注射部位和两个引流淋巴结的有效转染。(D) 体内外荧光和发光成像显示淋巴结中存在有效的选择性转染。(E) 用于 T 细胞反应分析的原代强化疫苗接种策略示意图,以及量化的 CD4+ 和 CD8+ T 细胞。
基于聚合物的递送系统为实现非病毒 mRNA 递送提供了另一种途径,该系统利用聚合物材料(其特点是分子量高,通常高达 10-106)通过基本结构单元的共价键结合形成的,如壳聚糖、聚乙烯亚胺(polyethylenimine ,PEI)和聚氨酯。其中典型的代表例子是 PEI 系统,它在向细胞递送 mRNA方面取得了巨大成功,此外,基于 PEI 的系统能够显著增强在皮肤外植体和小鼠体内自扩增 mRNA疫苗的反应能力。
聚合物纳米颗粒也被用于向免疫细胞输送 mRNA,尤其是用于体内 CAR T 细胞的应用。在一项研究中,Parayath 等人在循环 T 细胞中使用与抗 CD8 抗体结合的纳米载体,展示了体内CAR T的瞬时表达,从而避免了体外转染的需要,如下图所示。这些可注射的纳米载体可传递 IVT CAR 或 TCR mRNA,暂时重编程循环 T 细胞,使其靶向疾病特异性抗原。在这些纳米载体的设计中包含几个关键要素,包括表面锚定靶向配体、带负电荷的保护性涂层和便于选择性结合 T 细胞、防止降解和高效翻译编码蛋白质的载体基质。
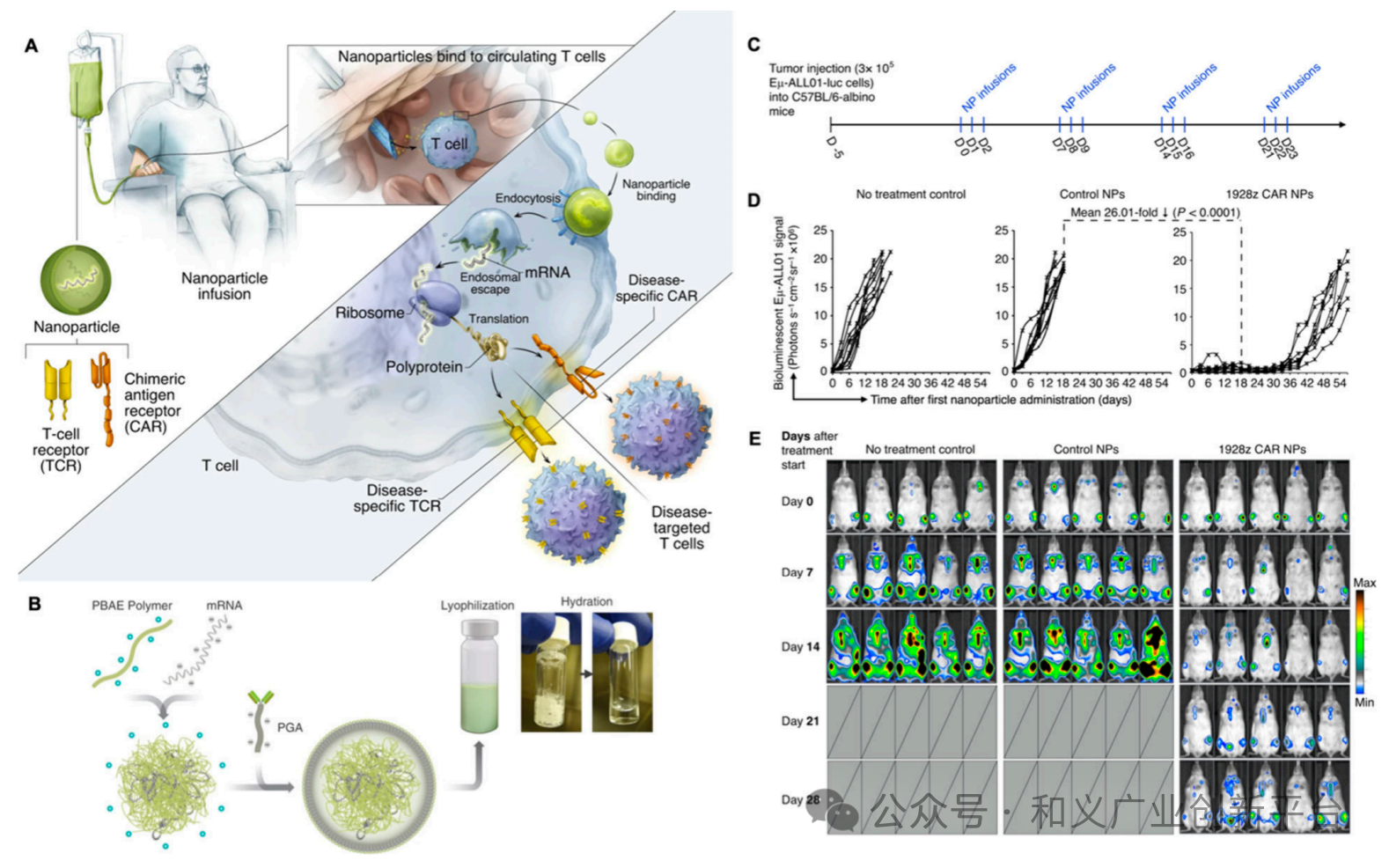
图. (A) 图解展示了通过聚合纳米颗粒递送的 IVT mRNA 对 T 细胞进行原位重编程,使其表达疾病特异性 CAR 或 TCR。(B)使用聚(β-氨基酯)、聚谷氨酸和抗 CD8 抗体合成聚合纳米颗粒的示意图。(C)给白化 C57BL/6 小鼠接种EU-ALL01 白血病细胞的剂量计划示意图。(D)纳米粒子给药后 Eμ-ALL01 荧光素酶信号强度图。(E)对注射了表达 Eμ-ALL01 白血病细胞的萤火虫荧光素酶的白化 C57BL/6 小鼠进行体内成像。IVIS 图像显示,施用携带 1928z CAR 的纳米载体可有效控制白血病的发展,与 GFP 对照组相比,治疗 3 周后肿瘤体积减小。
mRNA 纳米技术是一个取得突破性进展的研究领域,在疫苗接种、免疫调节和治疗免疫相关疾病方面具有巨大潜力。如今,140 多项临床试验正在探索 mRNA 治疗各种疾病(包括癌症和传染病)的潜力,利用 mRNA LNPs 刺激癌症免疫疗法中的免疫反应。由于免疫细胞对转染具有固有的抵抗力,因此要实现 mRNA 向免疫细胞的高效传递面临巨大挑战,必须采取量身定制的策略才能有效吸收。
要充分挖掘 mRNA 疗法的潜力,就必须采取新的方法来克服如免疫原性以及储存和运输过程中的稳定性等一系列障碍。免疫原性是外源 mRNA 有效递送的一大痛点,其一经引入可能会引发炎症和免疫激活,想要解决这一问题,须选择或设计具有可将免疫原性降至最低的生物材料。具有生物相容性的材料有望在避开先天性和适应性免疫系统检测的同时,将 mRNA 治疗药物输送到目标免疫细胞(既确保 mRNA 在储存和运输过程中保持稳定,又保持 mRNA 分子的完整性和功能性)。生物材料通过提供保护机制来保障 mRNA 的完整性,在这方面发挥着举足轻重的作用。将 mRNA 封装在保护性基质中并使用稳定剂,是延长 mRNA 保存期并在不同储存条件下保持治疗效力的有效策略。
声明:
翻译文稿不免出现笔误,还请各位读者指正和谅解!如有遗漏,欢迎留言补充。
整理丨武瑾嵘
排版丨壹 万
医疗器械、新材料、人工智能;
一定技术壁垒



