
对于老年人来说,修复因创伤、疾病和感染引起的大块骨缺损具有挑战性。当前尽管采用了最佳的临床实践方案,但在现有的外科植入合成支架中,骨再生往往存在问题。新兴的智能/多功能生物材料可能会影响与年龄相关的生物学衰退或在疾病/感染存在时的固有骨修复反应。该综述聚焦智能技术(这些技术在直接靶向和增强骨修复的能力方面具有良好的一致性),详细介绍了四种交互式智能支架体系。(本文只选取部分内容进行翻译解读,详细内容见附件原文)。

骨缺损通常与多种致病性疾病有关,包括创伤(骨折)、感染(骨髓炎和牙周炎)、肿瘤切除、骨质疏松症和其他骨科类疾病。基于骨移植的治疗方案包括自体骨移植、同种异体骨移植或异种骨移植,或通过使用脱矿化骨基质、生物陶瓷或金属支架。然而,自体移植存在供体部位发病率和吸收的问题;同种异体移植/异种移植存在免疫原性和疾病传播的风险;磷酸钙基陶瓷存在材料硬度和再吸收问题;金属植入物的腐蚀和细胞毒性离子的释放会引发炎症和过敏反应,进而导致骨质流失(如图所示)。
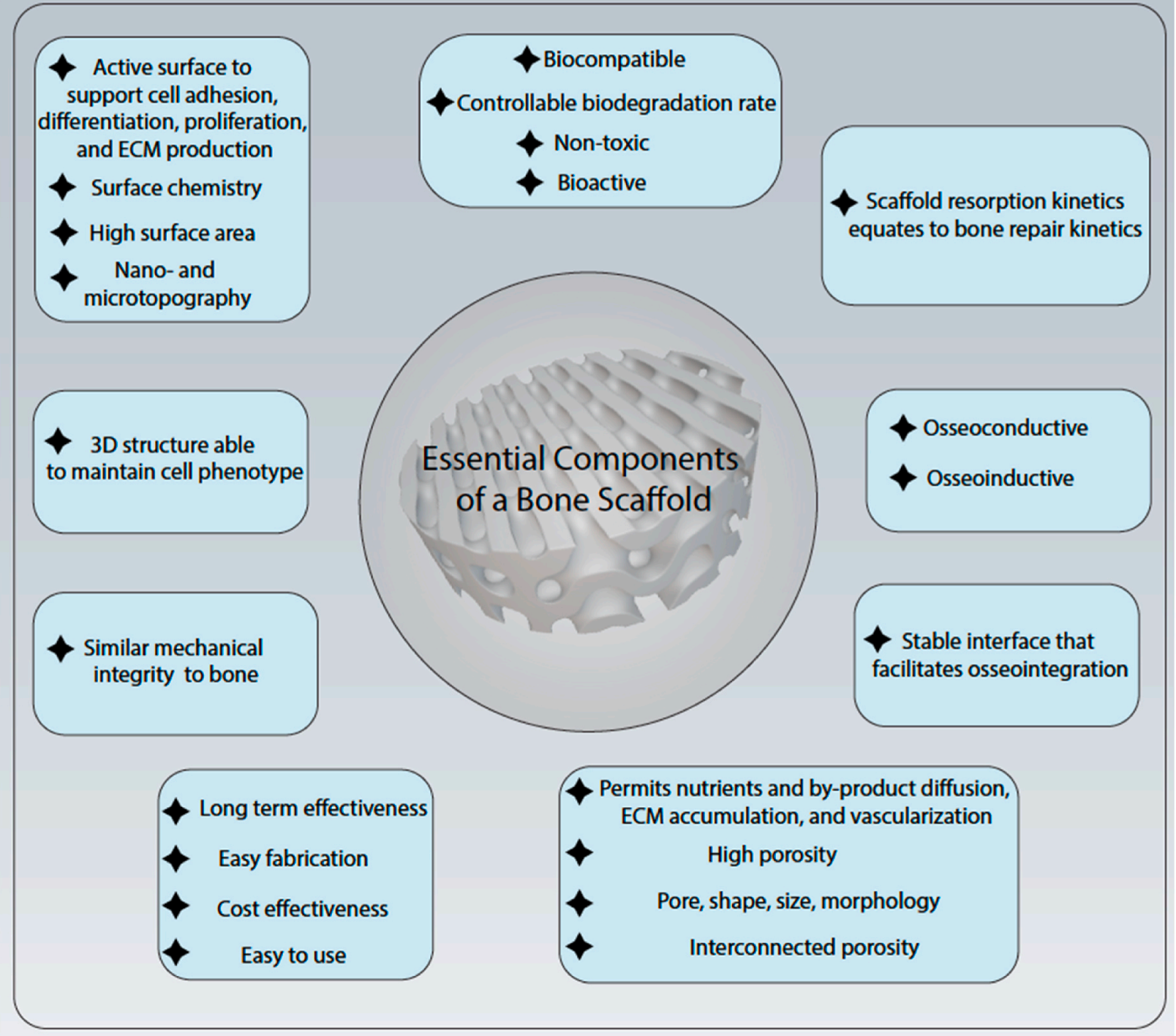
图. 合成骨支架所需的基本组成部分。包括生物相容性、生物可吸收性、成骨诱导性、结构和机械性能与天然骨相似的材料、易于使用且成本效益高。进一步的基本组成部分包括为细胞附着和生长提供最大表面积,运输营养物质和废物、适合血管生成的孔隙体积,以及可被吸收并替代骨的材料
无论损伤的位置或类型如何,骨组织修复都经历三个阶段:炎症、再生和重塑。虽然骨组织具有这种显著的自我重塑和修复能力,但在衰老过程中,由于生理变化的发生以及细胞内外环境的相互作用,细胞再生能力降低,老年患者的骨修复能力在传统骨疗法(如骨移植、Ilizarov技术、Masquelet技术)和生物活性合成支架材料(如脱矿质骨基质、磷酸三钙、羟基磷灰石)下是有限的。因此,多功能合成支架的设计可能为老年患者骨修复提供下一步发展。
2021年,Montoya等人重新定义了“智能生物材料”一词,并提出了四类智能度递增的类别:惰性、活性、响应性和自主性(如图所示)。在这项研究中,生物材料也被划分为两种:一种是通过其内部生物材料属性引发细胞微环境响应的智能材料,另一种是当应用于身体时,能对外部刺激做出响应的智能材料。
(1)惰性材料,生物相容但惰性的生物材料(如钛合金、不锈钢、陶瓷、聚合物等),其植入后显示出有限的功能,并且作为被动系统实施,没有适应和改变生物环境的能力;
(2)活性生物材料,通过化学修饰、表面电荷、孔隙性、刚度和离子渗漏等修饰方式增强活性生物材料的智能度,从而创造一个特定的支架环境,增强细胞间的交互和响应;
(3)响应性材料,是一种能够感知刺激并触发反应,实现信号分子的主动调节或特定药物释放的材料,这些刺激响应性或生物响应性材料能够感知体内特定刺激的存在(如pH、ROS、酶),或身体外部的信号(如电、磁或机械刺激),然后启动和执行特定功能;
(4)自主性材料,通过适应环境调整其活动,以响应生理环境内的变化,可提供精确、自给自足的支架活动(具有从微环境中处理信息的复杂能力,并改变其属性,以在长时间内提供针对性和剂量控制的治疗)。
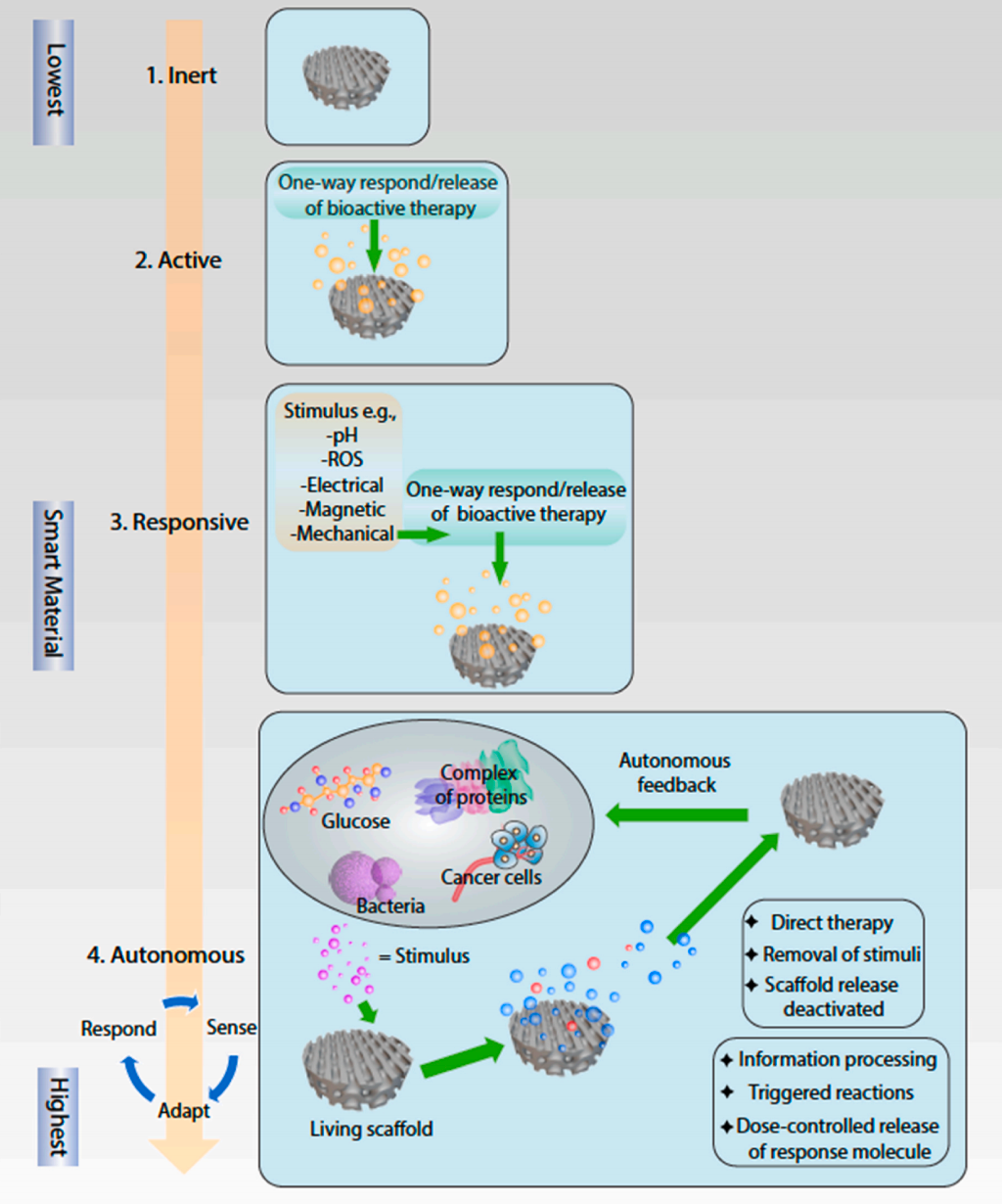
图. 生物智能度的四个层次。惰性、活性、响应性和自主性
人类衰老是一个多功能的、时间依赖的、不可逆转的细胞衰退过程,其特征是身体系统的形态、功能和生化发生改变。衰老的进展涉及多种因素,包括:(i)细胞核以及线粒体DNA损伤的积累;(ii) 核内不完整染色体的复制导致端粒磨损并随着细胞分裂不断积累,最终导致染色体完整性降低;(iii) 表观遗传基因组功能障碍;(iv) 错误折叠的蛋白质;(v) 细胞衰老。这些因素导致包括线粒体能量产生的效率低下,细胞损伤、细胞代谢及细胞分裂和组织再生的下降、细胞间通讯的改变。因此,这些细胞缺陷的总体积累导致功能障碍和健康生理过程的损害,如图所示。
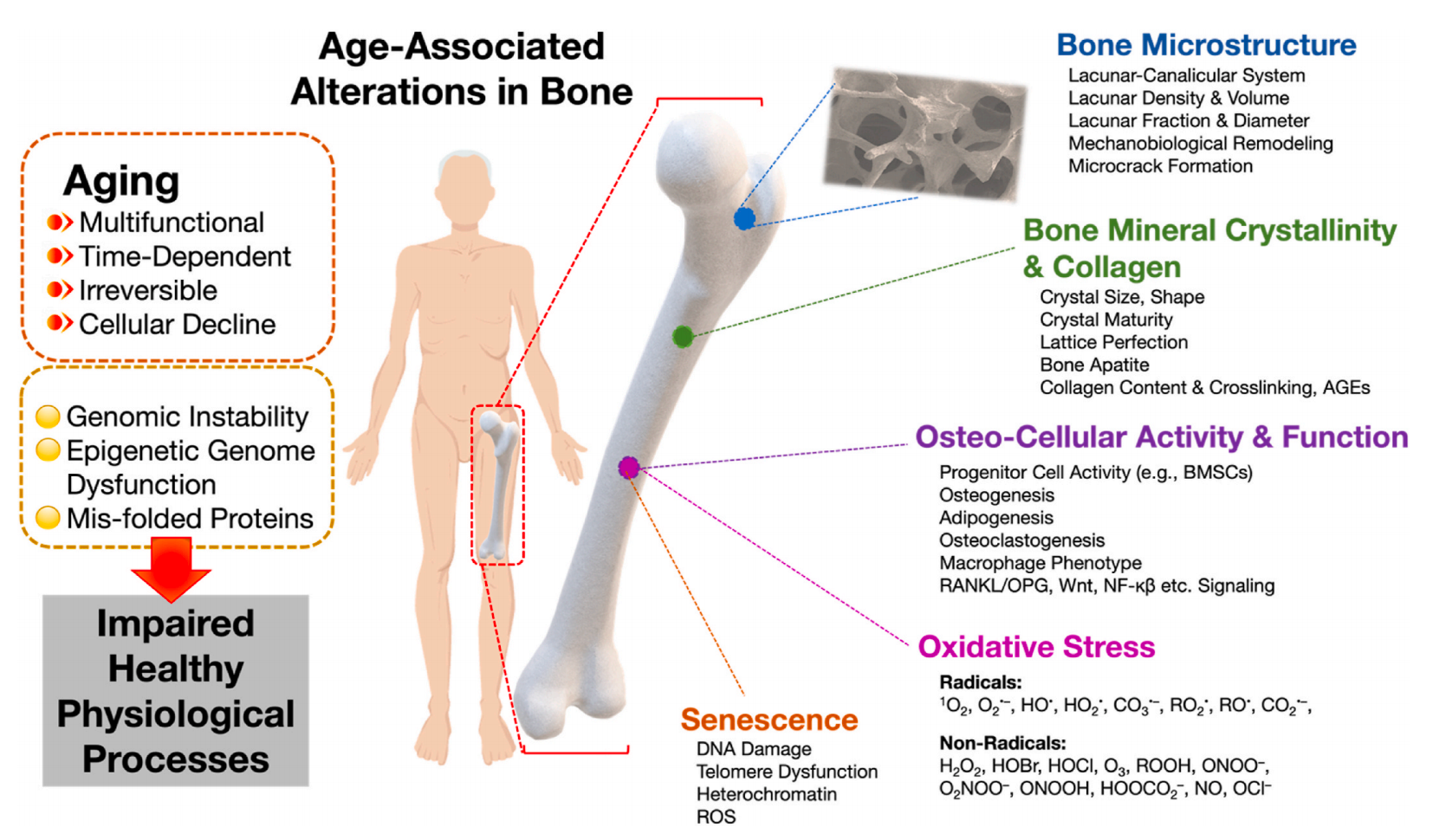
图. 在衰老期间影响骨骼健康的主要因素。如衰老会导致基因组不稳定、表观遗传基因组功能障碍和蛋白质错误折叠。骨骼因其微观结构的改变、矿物质结晶度和胶原蛋白含量与质量的变化、成骨细胞的活性和功能,以及增加的氧化应激和衰老而受到影响。这些因素共同阻碍成骨反应,影像骨组织在受伤后的自我重塑和自我修复能力。
总之,年龄相关的变化伴随着骨骼、细胞和新陈代谢活动中的变化,这些变化共同影响着骨矿物质和胶原蛋白的稳态,如图所示。重要的是,衰老是通过这些细胞和生物过程之间复杂的相互作用和反馈来调节的,如DNA 损伤的形成和积累,加上蛋白质质量的限制、受损或折叠错误蛋白质的有效清除,以及质量控制机制的减少,导致细胞器的缺陷;有缺陷的细胞器会积累更多的活性氧ROS,从而导致氧化应激、炎症和衰老,以及其他形式的细胞损伤,这些损伤和功能障碍共同降低了生物分子和细胞的质量。
因此,衰老的形成会促进炎症,反之亦然;同样,蛋白稳态的破坏会促进炎症,而炎症又会促进DNA 损伤,从而进一步加剧蛋白稳态的破坏。目前,这些生物过程之间在衰老和退化方面的相互作用仍有待全面发现,全面的了解能够提高对衰老机制的认识,同时新型的生物材料也能更好地预防或治疗与衰老相关的退行性疾病。总之,传统的单功能或双功能骨支架材料在修复由老化引起的大面积骨缺损时是有局限的。

图. 与年龄有关的主要变化
本篇文章摘录并翻译自:Multifunctional scaffolds for bone repair following age-related biological decline: Promising prospects for smart biomaterial-driven technologie,由于篇幅有限,余下译文内容将于明日推送。点击“阅读原文”查看原文链接。翻译文稿不免出现笔误,还请各位读者指正和谅解!如有遗漏,欢迎留言补充。
医疗器械、新材料、人工智能;
一定技术壁垒



