
概览:
美国食品药品监督管理局(FDA)表示,美敦力公司(Medtronic)召回了用于引流脑部液体的系统,原因是存在裂缝和泄漏的风险。
FDA发布了一份关于美敦力的Becker和Exacta外部引流和监测系统的1级召回通知,此前已收到15起相关伤害报告。FDA称,受影响的设备可能导致脑脊液泄漏、感染甚至死亡。
美敦力公司保留这些设备在市场上销售,但要求供应商检查其止水夹和连接处是否有可见裂缝。如果发现裂缝或泄漏,供应商应将设备退回美敦力公司。
洞察:
美敦力的Becker和Exacta设备为引流脑脊液提供了完整的封闭系统。这些设备还能让医护人员监测液体压力和流速。止水夹和连接处有助于液体流动。
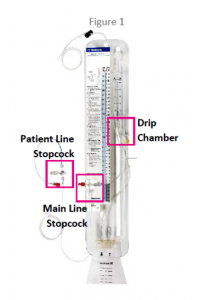
FDA的召回通知描述了设备止水夹存在裂缝和泄漏的风险。美敦力在11月收到客户关于止水夹的投诉后,向客户发送了通知。根据引流系统的配置,止水夹可能位于引流系统的三个不同部位。
尽管FDA表示目前尚未有患者因裂缝或泄漏而死亡,但潜在的严重伤害和死亡风险导致该机构将此次召回归类为最严重的类型。当美敦力在11月向客户发送通知时,公司表示已报告了3起与患者感染相关的不良事件。
美敦力已建议供应商按照产品标签上的建议,监测所有患者是否有感染迹象,并在使用过程中发现系统有裂缝或泄漏时继续监测患者。公司表示,有缺陷的设备应使用无菌技术进行更换。
FDA和美敦力还提供了如何防止泄漏的建议。公司建议,供应商应检查所有设备连接处是否紧密且无泄漏,但只能用手拧紧连接处。美敦力表示,过度拧紧连接处可能会导致裂缝和泄漏。
整理丨壹万
声明:以上内容根据公开资料整理,有遗漏,欢迎留言补充。
医疗器械、新材料、人工智能;
一定技术壁垒



