
虽然胰岛素泵可以模拟生理状态下的胰岛素的释放,但是耗材价格昂贵以及部分胰岛素泵佩戴不便等因素,胰岛素泵的渗透率长期较低。部分研究人员开始研究新型胰岛素递送系统,如:延长用药间隔的“胰岛素周制剂”以及对“非注射给药剂型”的探索,如胰岛素片剂、胰岛素胶囊以及胰岛素口腔贴剂。
口服胰岛素治疗
其难点主要集中于人体内物理、化学及酶作用三大屏障对药物吸收和稳定性的影响,使得胰岛素难以充分发挥治疗作用。生物利用度远低于注射给药。
➤化学屏障:pH等内环境可影响胰岛素结构的稳定性及作用;
➤酶作用屏障:蛋白酶可降解胰岛素,导致其生物利用度低;
➤物理屏障:肠上皮结构及功能对胰岛素吸收有阻碍作用,会抑制胰岛素的渗透/吸收。
许多工作试图使用纳米颗粒(NP)、水凝胶、脂质体和微球来制造口服胰岛素,但目前尚无一款药物获批上市[1]。跟多材料设计参见文献Material design for oral insulin delivery. 文中指出通过使用耐酸材料,包括合成聚合物材料、无机材料和MOF,可以克服恶劣的胃肠道环境。此外,zwitterionic和表面修饰载体已经证明了在动物模型中改善肠道渗透和提高生物利用度的能力。未来如何进一步提高生物利用度是研究重点。
目前,研发进度最快的口服胰岛素为ORMD-0801,其是一种口服重组人胰岛素肠溶胶囊制剂,采用肠溶包衣技术抑制小肠蛋白质水解作用,且添加吸 收增强剂以改善多肽通过肠道上皮内壁的能力,使胰岛素进入体循环。II b期临床研究证实 ORMD-0801对口服降糖药物疗效欠佳的T2DM 患者具有治疗安全性及有效性。天汇生物于2023年4月25日将ORMD-0801于国内申报上市 (CXSS2300021),其作为全球首个申报上市的口服胰岛素制剂备受瞩目,2023年8月2日Oramed公司宣布与天汇生物合资推进口服胰岛素商业化,未来口服胰岛素商业化将为 DM 患者带来新的治疗方案[2]。
胰岛素周制剂
新型超长效基础胰岛素制剂一周仅需注射1次,且低血糖事件少见,是新型胰岛素制剂的研究热点之一。目前在研但未上市的胰岛素周制剂包括美国的 PE0139、AB101、LY3209590,英国的单链胰岛素Fc融合变体,丹麦的 Icodec 胰岛素,韩国的 HM12460A、HM12470,以及中国公司的GZR4,其中,诺和诺德公司的 Icodec 胰岛素和礼来公司的 LY3209590研发进度最快。
·Icodec 胰岛素有望成为首款上市的基础胰岛素周制剂,是迄今为止研究最广泛、进程最快的胰岛素周制剂,诺和诺德公司已于今年提请上市申请。Icodec 胰岛素在人体内半衰期长达196 h,一周注射 1 次即可覆盖 1 周基础胰岛素需求,年注射次数约 52 次。Icodec 胰岛素与白蛋白亲和力较强而可逆,其与白蛋白的亲和力是地特胰岛素 (insulin detemir) 的9.5倍。
·LY3209590 BIF是一种融合蛋白,由一种新型胰岛素单链变体与人免疫球蛋白 G2 的 Fc 结构域融合组成,半衰期长达17 d。体外数据显示,BIF 较人胰岛素对人 IR 的结合亲和力弱 2 个数量级,但具有完全激动作用。
胰岛素透皮微针[3]
微针贴片由数十到数百根长度为数百微米的细针阵列组成,透皮时几乎没有痛觉,也不会留下明显创口,是一种理想的透皮给药方式。微针可以分为实心微针、涂层微针、空心微针、水凝胶微针和可溶性微针等。可溶性微针因为制备过程相对简单、载药量高、材料来源广、生物相容性好等优势在透皮给药方面具有良好的研究潜力,其中的药物被集成到微针的针体内,并随着微针的溶解而释放,药物利用率高,且不产生医疗废物。
截至目前为止,科研人员已开发出两大类葡萄糖响应性微针系统,即基于葡萄糖氧化酶的微针系统和基于苯硼酸的微针系统。
葡萄糖氧化酶是基于智能微针的胰岛素透皮给药系统方案中使用最广泛的葡萄糖传感材料之一。葡萄糖氧化酶是一种可以将葡萄糖氧化催化成葡萄糖酸和过氧化氢(H₂O₂)的酶。这一过程中的耗氧量会造成局部缺氧环境,可利用这一特性触发胰岛素给药,以应对高血糖。葡萄糖氧化过程中产生的H₂O₂也可以用于触发胰岛素从微针中释放。最后,葡萄糖酸的形成会导致局部pH值降低,通过在透皮给药系统中加入pH值敏感材料,也可以利用pH值降低来诱导胰岛素释放。因此,基于葡萄糖氧化酶的智能胰岛素透皮给药系统需要加入刺激响应性材料(对缺氧、H₂O₂或pH值),以实现葡萄糖响应性胰岛素释放。
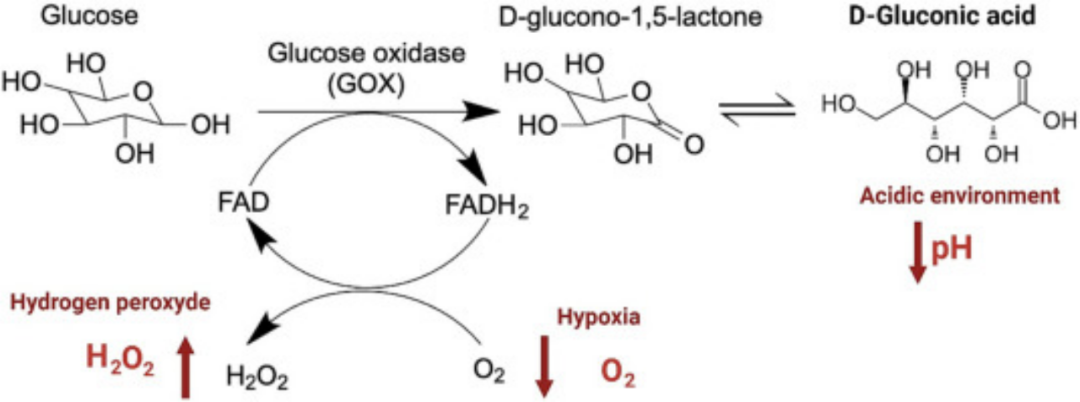
图. 葡萄糖氧化酶催化葡萄糖氧化的示意图,以及葡萄糖反应性胰岛素释放的独特刺激触发机制
基于苯硼酸的葡萄糖响应性微针贴片,以作为基于葡萄糖氧化酶的葡萄糖响应性微针贴片的替代品。苯硼酸是一种合成分子,由于其路易斯酸(Lewis acid)特性,它可以与葡萄糖等具有顺式-1,2或顺式-1,3二醇结构的化合物可逆地形成酯类物质,因此可以用作葡萄糖传感器。在水介质中,苯硼酸以不带电的三面体结构和带负电荷的四面体硼酸盐结构平衡存在。尽管这两种构型都能够与葡萄糖可逆结合并形成环状苯硼酸复合物,但带负电荷的硼酸盐结构的结合亲和力要高得多。因此,鉴于苯硼酸的pKa较高(8.6),在生理pH值(7.4)下,平衡主要偏向不带电的形式,从而导致葡萄糖响应性较低。因此,为了提高葡萄糖在生理pH值下的响应性,需要对葡萄糖响应性微针中的苯硼酸进行化学修饰,使其更具酸性,最终降低其pKa。为此,可以在苯硼酸的芳香环中引入吸电子基团(即卤素、硝基或羧基基团)和能够形成分子内配位键的正交取代基团(即在硼(B)与氮(N)或硼(B)与氧(O)之间)。迄今为止,已开发出的苯硼酸基微针系统的智能胰岛素给药机制包括电荷转换触发的溶胀、葡萄糖竞争性置换和交联解离。

图. 基于苯硼酸的葡萄糖反应胰岛素输送机制的示意图:a)电荷开关引发的溶胀,b)竞争性位移和c)交联解离
总结:胰岛素泵目前的发展趋势实现闭环输送胰岛素,小型化、便携化、智能化来提升用户体验也是目前的行业共识。贴附式泵可能是未来主要竞争重点。各厂家无论是通过与CGM厂商进行合作或者自己开发血糖监测系统,最终目的是为了能够更好模拟人体胰腺的功能,控制患者的血糖水平处于正常状态。开发新型泵体降低成本,或者改进胰岛素递送方式是目前研究的热点。国际厂商同时也在通过收并购积极布局胰岛素患者监测、治疗、管理上下游产业链,逐渐形成全产业链的产品结构布局。
声明:以上根据公开资料整理。如有遗漏,欢迎留言补充。
作者:DU
医疗器械、新材料、人工智能;
一定技术壁垒



