
细胞自噬最早由Ashford和Porten于1962年用电子显微镜在人的肝细胞中发现,广泛存在于真核细胞内,也是为细胞维持生存的一种重要机制。
研究发现,自噬对于肿瘤细胞存在促进与抑制的双重作用。一方面,自噬能在不利环境中提高肿瘤细胞对应激的耐受能力,维持其生存;另一方面,自噬又能在肿瘤发展的不同阶段抑制其产生和转移,甚至成为某些凋亡缺陷肿瘤细胞的死亡途径。
自噬调节可能成为一种新的与传统细胞毒性药物或靶向试剂相关的抗癌疗法。
研究摘要
光动力疗法 (PDT) 期间产生的活性氧 (ROS) 可诱导细胞自噬,以保护肿瘤细胞免于凋亡。在这项工作中,研究者开发了一种自我递送自噬调节因子(称之为 CeCe),由光敏剂(Ce6)和自噬促进剂雷公藤红素组装而成。
Ce6 和雷公藤红素能够自组装成具有良好光动力性能和自噬调节能力的纳米药物。在光照下,CeCe会在肿瘤细胞中产生ROS,放大氧化应激,促进细胞自噬。因此,CeCe表现出强光毒性。
体内实验表明,CeCe可以在肿瘤组织中聚集,从而获得良好的PDT效果。
研究也证明了PDT 和自噬相促进的协同抗肿瘤作用。这种自递送纳米药物可能会促进共递送纳米平台的开发,以通过促进自噬来提高 PDT 的抗肿瘤功效。
背景简介
雷公藤红素是一种自噬促进剂,它还可以有效地产生 ROS 以抑制肿瘤。
然而,其较强的疏水性和全身副作用限制了其在生物医学中的应用和治疗效果。
团队研究了光敏剂和自噬促进剂的协同抗肿瘤作用,并开发了一种自噬调节剂(称之为CeCe)。
如下图所示,CeCe 是由光敏剂(chlo- rin e6, Ce6)和自噬催化剂(雷公藤红素)通过π -π堆积和疏水相互作用自组装而成。
结果发现,CeCe 不需要药物载体,但粒径分布均匀,稳定性较好。此外,CeCe 能够优先在肿瘤组织中积累并提高药物递送效率。同时,CeCe 可以产生 ROS 和提高自噬水平以启动自噬细胞死亡。
有益的是,氧化应激和自噬性细胞死亡增强了 PDT 的抗肿瘤作用。体外和体内研究结果均表明,CeCe 可以逆转肿瘤细胞的 PDT 抗性,并显着增强协同肿瘤抑制作用。
自我递送生物医学通过促进自噬将PDT放大,为肿瘤协同治疗的临床应用提供了新的思路。
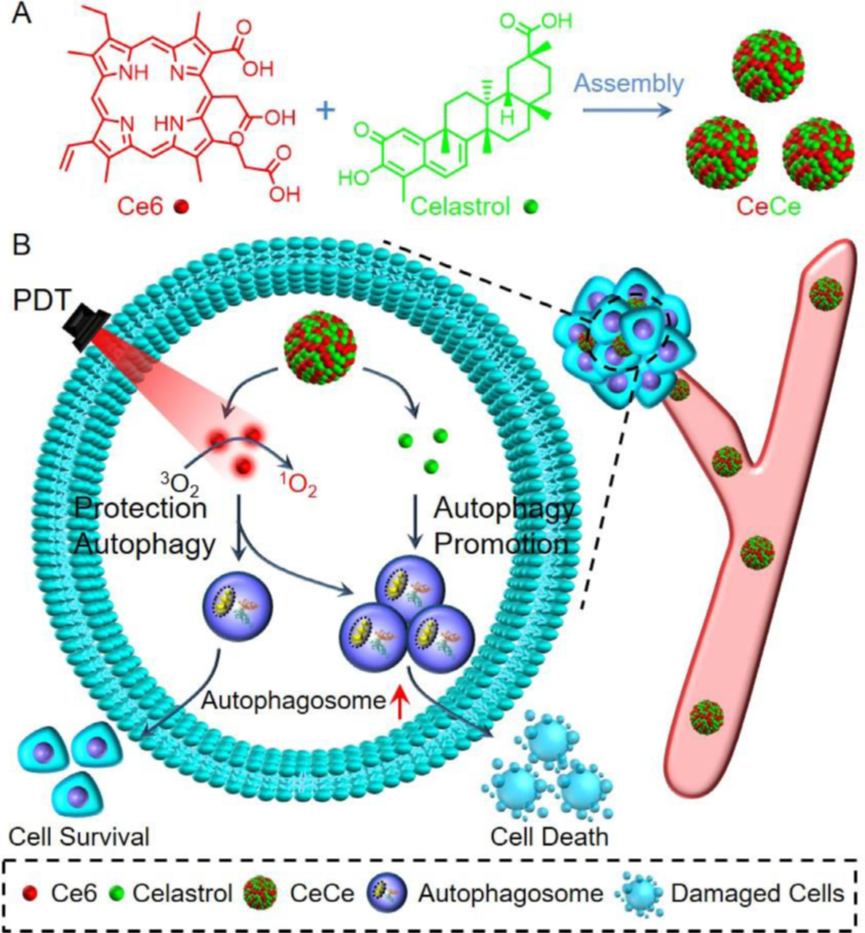
(A) CeCe 是通过 Ce6 和 雷公藤红素 的组装制备的。(B) 静脉注射的 CeCe 在肿瘤部位积聚用于细胞内化。随后,释放的 Ce6 产生单线态氧以放大细胞氧化应激并促进自噬。此外,雷公藤红素作为自噬促进剂可诱导自噬细胞死亡。因此,CeCe 通过 PDT 和自噬促进的协同作用表现出更强的抗肿瘤能力。
研究内容
1. CeCe的制备和表征
选择 Ce6 和雷公藤红素作为光敏剂和自噬促进剂,在不含任何载体的情况下进行自组装。通过TEM和动态光散射(DLS)表征了形貌和粒径。为了说明自组装的机制,利用紫外-可见分光光度计测定了CeCe在不同条件下的特征吸收峰的变化。观察到疏水性相互作用可能是自组装的驱动力。
此外,与单体 Ce6相比,CeCe 具有明显更宽且红移的 Q 带,这可归因于π -π堆叠。此外,不同浓度的氯化钠(NaCl)溶液处理后,CeCe的吸光度变化很小,这表明在自组装过程中,静电作用可以忽略不计。
这些结果表明,Ce6和雷公藤红素自组装的驱动力主要是π- π叠加和疏水相互作用。
2. CeCe的体外抗肿瘤作用研究
通过MTT法、细胞凋亡分析和活/死染色法研究CeCe的体外抗肿瘤作用。
首先,CT26 细胞的活力和完整性在光照射下没有受到影响,这证实了光对肿瘤细胞的影响可以忽略不计。此外,Ce6 在黑暗中具有较低的细胞毒性,因为在没有激光照射的情况下,PDT 无法发挥其肿瘤杀伤活性。
尽管雷公藤红素和 CeCe 可以降低细胞活力,但它们的毒性较小。而当有光存在时,CeCe对CT26细胞表现出浓度依赖性的光毒性,抑制率非常高(超过90%)。
此外,Ce6 和雷公藤红素的混合物在光存在时比 Ce6 具有更强的细胞毒性,这证实了雷公藤红素诱导的自噬和 Ce6 介导的 PDT 的协同抗肿瘤作用。
随后,通过流式细胞术(相关文章推荐阅读:什么是流式细胞仪?一文带你了解流式细胞仪检测原理、组成结构...)进行细胞凋亡检测。在无光条件下,雷公藤红素组、Ce6 +雷公藤红素组和CeCe组约有25- 30%的细胞发生凋亡。特别值得注意的是,一旦暴露在光照射下,细胞凋亡率就会急剧增加。其中CeCe组细胞凋亡率最高,超过90%,其次是Ce6+雷公藤红素组,Ce6组最低。
此外,使用 CLSM通过活/死染色测定直观地观察细胞状态,其产生与流式细胞术分析一致的结果。尤其在光照组中观察到绝大多数的死亡细胞,其中CeCe组在视野中几乎全部显示红色PI荧光。
上述结果说明了 CeCe 介导的PDT的强大抗肿瘤作用,证明了自我递送纳米药物在肿瘤协同治疗中的优势。
3. CeCe对自噬致敏PDT机制的研究
为了进一步研究 CeCe 的协同抗肿瘤机制,研究者深入研究了 CeCe 介导的促死亡自噬。
如图所示,在用雷公藤红素和 CeCe 处理的 CT26 细胞的 Bio-TEM 图像中观察到更多的自噬体,表明发生了自噬。此外,细胞酸性自噬囊泡通过 MDC 染色测量。用MDC处理后,自噬囊泡可以发出绿色点状荧光。与空白对照相比,尽管缺乏光照,但雷公藤红素和 CeCe 组的绿色荧光增加。
此外,尽管 Ce6 PDT 后的 CT26 细胞也表现出增强的荧光,但经Ce6光动力治疗后的细胞内囊泡最多。
结果表明,CeCe 介导的 PDT 可以在雷公藤红素的帮助下提高自噬水平,这可以通过雷公藤红素和Ce6 的协同作用来解释。
此外,在明亮的视野中,Ce6比CeCe在光照下诱导的细胞形态改变更少,进一步表明CeCe能够逆转pdt诱导的细胞保护性自噬,从而增强促死亡自噬。同时,定量荧光分析还证实,雷公藤红素辅助 PDT 协同上调自噬水平。
接下来,通过蛋白质印迹检测自噬标记蛋白 LC3。
一般情况下,LC3通常以可溶性LC3-i的形式存在于细胞质中,但它可以在自噬过程中转化为LC3-ii,然后在泛素修饰后聚集在自噬体膜中。
如图所示,在用雷公藤红素、CeCe 或 Ce6 + 雷公藤红素处理后,LC3-II表达上调。同时,定量分析还表明 LC3-II/LC3-I 的比例增加。
值得注意的是,Ce6 介导的 PDT 促进 LC3-II 表达的程度较小,而 CeCe 介导的 PDT 显着放大了 LC3-II / LC3-I 比率。免疫荧光技术检测细胞内LC3点状分布。
如图所示,光照下的雷公藤红素和 Ce6 均可引起荧光增强,但 CeCe 介导的 PDT 导致最多数量的绿色点状点。显然,雷公藤红素和PDT均可诱导细胞自噬,而CeCe在光照下可进一步促进细胞自噬水平。
此外,通过使用自噬促进剂(雷帕霉素,Rapa)和自噬抑制剂(3-甲基腺嘌呤,3-MA)进一步研究细胞自噬与PDT之间的关系。如图所示,3-MA处理后Ce6的抗增殖能力下降,而Rapa处理后Ce6的PDT作用增强。
此外,还观察到 3-MA 可以增强羰基化蛋白质的积累,但 Rapa 减少了这种蛋白质修饰。基于以上结果,可以推断,PDT诱导的自噬维持在较低的基础水平,在PDT过程中起到细胞保护作用。如图所示,3-MA处理后Ce6的抗增殖能力下降,而Rapa处理后Ce6的PDT作用增强。

(A) TEM 图像(比例尺:5 μm)和放大图像(比例尺:2 μm),显示与 Ce6、雷公藤红素或 CeCe 孵育后 CT26 细胞的自噬体(红色箭头)。(B) MDC 染色和 (C) CT26 细胞在有光或无光条件下用 Ce6、雷公藤红素、Ce6 + 雷公藤红素 或 CeCe 处理后的平均荧光强度 (MFI) 分析 (n = 3)。比例尺:10μm。(D) Western blot 和 (E) 在存在或不存在光的情况下,用 Ce6、雷公藤红素、Ce6 +雷公藤红素或 CeCe 处理后 CT26 细胞中 LC3 表达的定量分析 (n = 3)。(F) 在有或没有光的情况下用 Ce6、雷公藤红素、Ce6 +雷公藤红素或 CeCe 处理后 CT26 细胞中 LC3 点状点的 CLSM 图像。
4. CeCe的体内抗肿瘤研究
大量研究表明,自组装的纳米颗粒更倾向于通过EPR效应在肿瘤组织中聚集。
在研究CeCe的体内抗肿瘤作用之前,研究者通过小动物成像系统研究了CeCe的生物分布。
如图所示,在CT26荷瘤小鼠静脉内注射CeCe后,观察到CeCe随血液循环分布于全身。
之后,随着时间的推移,荧光主要在肿瘤组织中积累,表明 CeCe 具有被动的肿瘤靶向能力。6小时后,由于体内的生物代谢,肿瘤部位的荧光逐渐消失。肿瘤区域平均荧光强度的测量与上述结果一致。
术后12小时处死小鼠,另外取肿瘤组织和主要脏器进行离体显像。尽管部分CeCe已被肝脏代谢,但由于肿瘤滞留能力,仍可在肿瘤组织中发现荧光聚集。实时荧光成像结果说明了 CeCe 的肿瘤靶向能力,这将有助于提高抗肿瘤效果。
此外,使用 CT26 肿瘤模型进行动物实验以评估 CeCe 在体内的抗肿瘤功效。
荷瘤小鼠通过尾静脉注射给药,6小时后暴露于激光照射。之后每2天监测一次肿瘤体积和体重变化。
如图所示,当没有光处理时,Ce6 对肿瘤生长没有影响。此外,CeCe的抑瘤作用强于雷公藤红素,这与雷公藤红素通过自组装提高生物利用度和药物溶解度有关。
此外,CeCe 在光照下表现出比 Ce6 和雷公藤红素联合治疗更强的肿瘤生长抑制作用,表明 CeCe 通过自噬促进致敏 PDT 增强了协同抗肿瘤作用。小鼠体重监测过程中,未发现明显波动,这意味着这些抗肿瘤药物在治疗剂量下具有低全身毒性。同时,在治疗结束时收集肿瘤进行拍照和称重。可以看出,用 CeCe 和光处理的组中的肿瘤最小,表明自噬致敏 PDT 具有强大的抗肿瘤作用。
此外,肿瘤组织用 TUNEL 和 H&E 染色。
如图所示,在经CeCe和光处理的肿瘤中,TUNEL显示出最亮的绿色荧光,表明CeCe可以最大程度地促进肿瘤细胞的凋亡。同时,H&E 染色分析表明,CeCe 的 PDT 后发现大量无细胞核的细胞,表明由于自噬细胞死亡和光动力细胞凋亡的协同作用,具有强大的抗增殖活性。
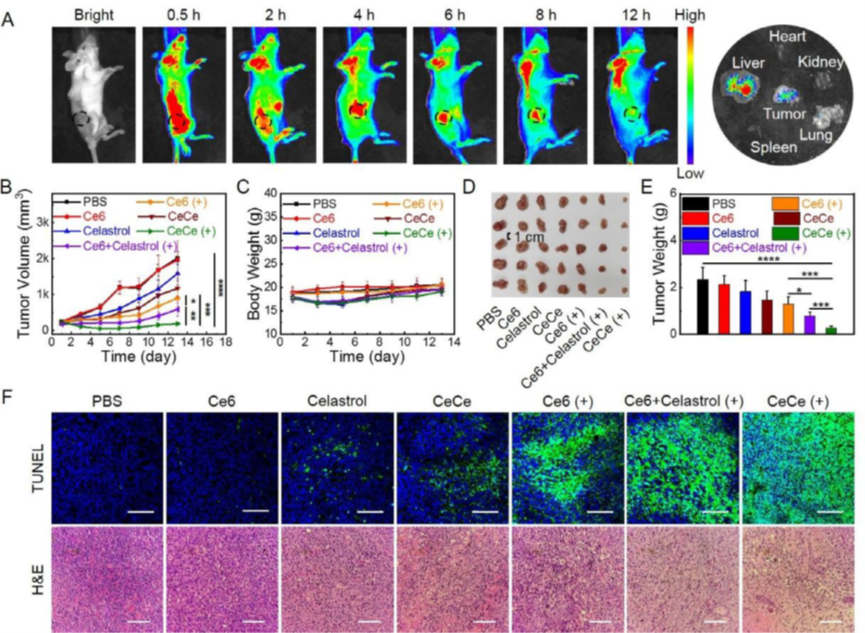
(A) CT26 荷瘤小鼠静脉注射 CeCe 后的体内实时荧光图像和给药后 12 小时后的离体组织成像。(B) 在存在或不存在光照的情况下,在 13 天内 (n = 5),小鼠在给予 Ce6、雷公藤红素、Ce6 +雷公藤红素 或 CeCe 后的肿瘤生长曲线和 (C) 体重变化。(D) 处死小鼠的肿瘤组织和 (E) 第 13 天小鼠的平均肿瘤重量 (n = 5)。(F) 第 13 天肿瘤组织的 TUNEL 和 H&E 染色分析。
结论
这项研究报告了一种通过促进自噬菌以增强 PDT 的自我递送生物医学 (CeCe)。基于合适的投料比,Ce6和雷公藤红素在没有任何赋形剂的情况下自组装成均匀的纳米药物,避免了载体的过量毒性。
此外,无载体CeCe表现出合适的粒径,以及在水溶液中良好的稳定性和分散性。同时,CeCe 具有更好的光动力性能、自噬调节和抗肿瘤能力。重要的是,CeCe 通过促进 ROS 的产生来提高自噬水平,从而放大细胞内的氧化应激。
另一方面,自噬的过度激活引起自噬性细胞死亡,可以逆转肿瘤细胞对PDT的抵抗,从而增强PDT疗效。静脉注射后,CeCe通过EPR效应优先在肿瘤组织中蓄积,进行靶向治疗。
最后,CeCe 显著抑制肿瘤生长,体内副作用可忽略不计。
综上所述,本研究证明了自递送自噬调节剂的强大抗肿瘤作用,为光动力协同肿瘤治疗提供了新的手段。
封面图来源:图片来自网络,侵删
作者声明:感谢本文参考资料作者,文中观点仅供参考,不恰当之处还望包涵指正,资料内容侵删。
作者:叶瑞霆
审核:晓 柏
排版:大大怪
医疗器械、新材料、人工智能;
一定技术壁垒



