
4月17日,北京市医保局、北京市发改委、北京市药监局等9部门联合印发《北京市支持创新医药高质量发展若干措施(2024年)》。该措施从创新药械研发、临床实验、审评审批、生产制造、流通贸易、临床应用等八个方面提出32条举措。本篇将继续解读北京市创新医药32条政策要点。
【大力促进医药贸易便利化】
(一)政策原文:
1.争取国家相关部门支持,在北京天竺综合保税区建立罕见病药品保障先行区,实施罕见病药品“白名单”制度(罕见病药品、试点医疗机构、进口药品经营企业三个“白名单”),打通一次审批、多次进口、多家医疗机构使用的绿色通道,2024年力争推动10个品种全环节打通落地。
··罕见病药品保障先行区
于2023年11月,《支持北京深化国家服务业扩大开放综合示范区建设工作方案》国务院批复建立。主要以存储未在国内注册上市的罕见病(209种)进口药品,可由特定医疗机构指导药品使用。

图:北京日报 天竺综合保税区一公司仓储人员进行药品库内养护
该区运营模式参考海南博鳌乐城国际医疗旅游先行区及《粤港澳大湾区药品医疗器械监管创新发展工作方案》,即“港澳药械通”政策。
··海南博鳌乐城国际医疗旅游先行区
于2013年2月28日经国务院批准设立,并被赋予九条优惠政策,园区试点发展特许医疗、健康管理、照护康复、医美抗衰等国际医疗旅游相关产业,形成为游客提供体检、健康管理、医疗服务、康复、养生(护)等完整的医疗产业链。旨在聚集国际国内高端医疗旅游服务和国际前沿医药科技成果,创建国际化医疗技术服务产业聚集区。
2019年9月16日,国家发展和改革委员会、国家卫生健康委员会、国家中医药管理局、国家药品监督管理局四部委联合发布《关于支持建设博鳌乐城国际医疗旅游先行区的实施方案》。区内特定医疗机构因临床急需,进口在海外已批准上市但尚未在我国获批的、国内已注册品种无法替代的药品。
··“港澳药械通”政策
指定医疗机构使用临床急需、已在港澳上市的药品,以及临床急需、港澳公立医院已采购使用、具有临床应用先进性的医疗器械。已在港澳上市的罕见病治疗药物,可借助“港澳药械通”经审批后在大湾区内使用。
截止目前指定医疗机构有中山大学附属第一医院、广东省人民医院、南方医科大学南方医院、广州市第一人民医院南沙医院等。
(二)政策原文:
1.进口:优化药品进口通关抽样一体化服务,实现24小时通关便利化,2024年增加进口药品品种5个以上。
2.出口:推动企业更广泛深入参与国际合作,建立对外交流平台,优化药品出口流程,2024年推动5个品种“走出去”。
主要负责单位:市药监局、北京海关、市商务局
【促进创新医药临床应用】
对创新技术项目优先启动统一定价论证程序,同步研究纳入医保支付。优化药品阳光采购挂网流程,完善创新医疗药械绿色通道机制,实现快速挂网。对已批准设立的新增医疗服务价格项目,医疗机构可随时备案并开展应用。
政策利好:对创新技术项目优先启动统一定价论证程序,同步研究纳入医保支付。进一步减少审批环节,优化审批流程,受理周期从每半年缩短到每季度,创新医疗器械产生的新医疗技术、新医疗活动不受受理周期限制,可通过绿色通道随时申报。
工作进展:已为43个创新药品实现快速挂网,包括培莫沙肽注射液、托莱西单抗注射液等29个国产药品,还包括注射用维泊妥珠单抗、甲苯磺酸利特昔替尼胶囊等进口药品。
··新增医疗服务价格项目
创新医疗技术、服务在临床应用时,没有对应的收费项目,则需要到市医保局申报。
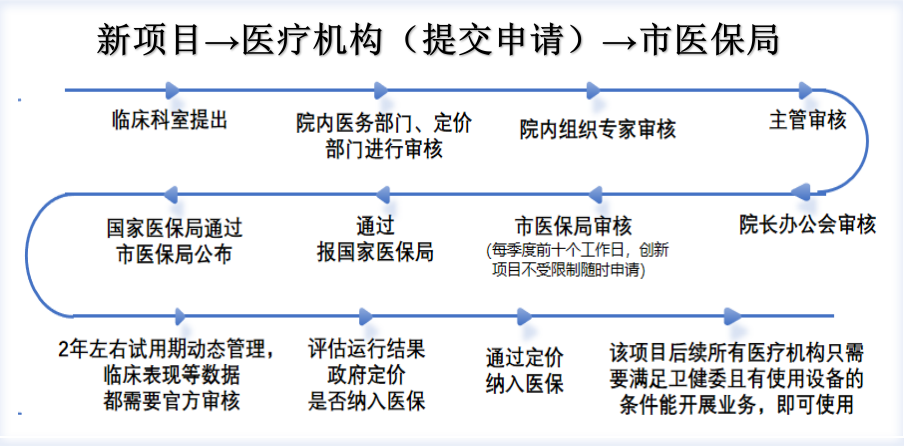
项目申报流程
(仅作参考,具体请以海淀区医保局为准联系电话:医药服务监管科88506508)
医疗机构是指公立医疗机构,会评估项目的申报成功率(经济性、创新性)再决定是否备案,一般第一个申报的医疗机构都是三甲医院带头,医院院内相关部门对该申报项目流程都非常了解。
目前申请的情况来看,市医保局反馈项目质量不高,体现在创新性不高、申请报告书写不精准等均会影响新项目审批。
(二)政策原文:
取消医疗机构药品数量限制。推动建立医疗机构药事会规范化流程,国谈药目录公布后一个月内召开药事会,全年药事会召开不少于4次。
政策利好:之前不同级别的医院用药目录种类数量的限制,如在国家三级医院等级评审指标中,三级综合医院原则上不超过1500种药品。
··药事会
定义:对医院药品管理的重大事务进行讨论和表决的机构,所有涉及药事管理政策和药品遴选事项均须经过药事会集体讨论通过。
主要职责:研究我国医疗机构药事管理的发展现状,提出政策建议,以及推动药物治疗相关临床诊疗指南和药物临床应用指导原则的实施。药事委员会还负责选择满足临床需要的药物,遵循购药三优先原则:进口药品优先、儿童专用剂型优先、大厂大品牌药品优先。
日常召开会议谈论内容,医院是否需要进,是否调整药,以及创新药是否适合临床使用等等。
(三)政策原文:
《中关村创新医疗器械产品目录》按季度更新。推进《中关村创新医疗器械产品目录》和首台(套)重大技术装备目录产品进医院,实施创新药械“随批随进”。
··首台(套)重大技术装备——国家工信部
相关政策文件:《首台(套)重大技术装备推广应用指导目录(2019年版)》
最新政策项目进展:北京发改委4月起征集2024年首台(套)重大技术装备产品
具体官网通知:关于征集2024年首台(套)重大技术装备产品的通知
https://www.beijing.gov.cn/zhengce/zhengcefagui/202404/t20240423_3632562.html
内含各区首台(套)产品申报单位联系表
申报流程:随时申报,季度评审
申报负责单位:北京市首台(套)重大技术装备统筹联席会办公室
(四)政策原文:
国谈药和创新医疗器械涉及的诊疗项目,不受医疗机构总额预算指标限制;对需要开展绩效考核和总额预算管理(BJ-GBI)质量评价的医疗机构,剔除国谈药、创新诊疗项目对人均药品费用、人均医疗费用等相关指标的影响。
主要负责单位:市医保局、市卫生健康委
(五)政策原文:
支持建立医用机器人等创新器械应用培训中心,加快创新医疗器械推广使用。
主要负责单位:市科委中关村管委会、市经济和信息化局、市医管中心、市卫生健康委、相关区政府
【强化创新医药企业投融资支持】
(一)政策原文:
用好北京市医药健康产业投资基金,带动社会投资,推动一批具有战略性、前沿性的全球原创技术和品种在京转化,支持一批有重大潜在产值贡献的创新药械、细胞与基因治疗、数字医疗等领域产业项目落地并实现产品快速上市。
主要负责单位:市科委中关村管委会、市经济和信息化局
··北京市医药健康产业投资基金
北京市政府投资引导基金联合社会资本组建设立200亿医药健康产业基金,落地昌平。其中引导基金出资不超过70亿元。基金可分两期实施,首期目标规模100亿元。
基金重点投向创新药、创新医疗器械等重点产业领域以及细胞与基因治疗、数字医疗等新兴产业领域,兼顾公共卫生安全、临床生产服务等领域。
管理机构于23年9月在社会征集,最终由北京市政府投资引导基金管理有限公司、北京京国管置业管理有限公司、北京康士达管理咨询有限公司,及关联机构康桥资本共同管理。
··康桥资本(CBC Group)
康桥资本成立于14年,是亚洲一家专注于医疗健康行业投资的资产管理公司,目前总资产管理规模超过88亿美元。
旗下有私募基金、康桥医疗健康产业设施平台、瑞桥信贷基金等。
主导和深度参与了云顶新耀、苏桥医药、优锐医药、安瑞医疗、道培医院、AffaMed、NiKang等多家医疗行业创新企业的发展。
(二)政策原文:
引导金融体系为初创期创新医药企业提供创业投资、担保增信,推动更多资金投早、投小。综合运用知识产权和股权质押融资、研发贷、供应链金融等产品,推动成长期创新医药企业扩大生产、创新研发、成果转化。优化传统信贷、跨境投融资、投行并购等综合业务,提升成熟期创新医药企业金融服务适配性。相关银行发放贷款、贴现符合“京创融”、“京创通”政策要求的,优先给予支持。
主要负责单位:市委金融办、人民银行北京市分行、国家金融监督管理总局北京监管局、北京证监局、市医保局、市科委中关村管委会、市经济和信息化局
声明:
本文根据公开资料整理。如有遗漏,欢迎留言补充。
排版丨壹 万
医疗器械、新材料、人工智能;
一定技术壁垒



