
和义广业【行业分析】医用镁合金系列,将分析生物可降解金属之一镁基金属及合金的特性、应用研究进展、医学应用层面的性能指标检测以及相关代表公司情况等。本篇列举了一些目前常用的检测性能的基本方法,并对从ClinicalTrials数据库中检索出的临床试验资料进行简述。
▍镁基金属性能检测指标方法
开发新的镁基生物材料,需测试和评估其物理化学性能,以评估这些修饰的功效。下面列举了一些目前常用的检测性能的基本方法,如何选择选择合适的测试以及适当的实验条件对镁基材料的性能评价尤其重要。
1 体外腐蚀实验检测方法以及影响因素 [1]
在进行基础研究时,有多种体外腐蚀实验方法可观测镁合金的体外降解速率,如:电化学腐蚀试验、浸泡实验、氢气释放速率。对于体外腐蚀实验,所用的介质溶液会影响降解速率。所以需要选择合适的实验方法以及合适的溶液介质进行检测。
1)电化学腐蚀试验(Electrochemical corrosion test)
通过使用参比电极、读数器和工作电极的三电极系统监测开路电位 (OCP)、极化(polarization)和电化学阻抗谱 (EIS) 来评估腐蚀速率。
利用动电位极化提供腐蚀电位(Ecorr)和腐蚀电流密度(Icorr)的数据。由于金属间化合物或填料颗粒等第二相的存在,普通镁合金不会表现出均匀的腐蚀模式。只有假设均匀腐蚀,才能将 Icorr 转换为腐蚀速率 (CR)。因此,动电位极化测试结果通常不会产生准确的CR。
当金属表面暴露在电解质溶液中时,需要一定的时间在表面形成双电层,然后才能稳定下来。对于镁合金,OCP 时间约为15-20 min,-150 到 + 500 mV是一个合适的电位范围。
在EIS(电化学阻抗谱)测试中,频率范围有重要影响。如果电极系统足够稳定,频率应该足够低以使测量时间更长。另一方面,如果电极系统是活性的,则在长时间的测试中,表面特性会发生变化,数据的可信性降低。因此频率应较高,而测试时间较短,一般选择100khz ~ 10Mhz。
2)浸泡试验
浸泡试验是评价可降解金属材料腐蚀性能的常用方法。根据ISO 10993-15(医疗器械的生物学评估-第15部分:金属和合金降解产物的鉴定和量化)和ASTM G31-72(金属实验室浸没腐蚀测试的标准),来确定镁合金质量变化、氢气析出、pH变化、Mg离子释放和腐蚀产物。影响腐蚀结果的因素包括溶液体积与试样比表面积(V/S)、流速、浸泡时间和腐蚀速率的评价方法。
在生物环境应用的基础上选择模拟溶液和V/S比是非常必要的。例如,选择高V/S比(如6.7)和低V/S比(如0.67)来模拟镁骨螺钉在骨髓腔和镁植物中的体内降解行为——分别拧入皮质骨或肌肉组织。
3)检测H2的释放速度
H2 释放反映了腐蚀动力学,可用于评估镁合金的腐蚀速率,这是因为 :
- H2 释放是镁金属植入后的破坏性过程;
- 析出H2的摩尔值与溶解Mg的摩尔值完全相等,因此H2析出速率可以准确反映镁的腐蚀速率;
- 1摩尔放出的H2相当于溶液中产生2摩尔OH-,因此放出H2的速率表示溶液中发生的碱化速率。目前镁合金的H2释放速率为每天 0.01 ml/cm2作为耐受水平,可用作进一步体内实验的依据。
4)测定溶液中镁离子的释放量:
采用电感耦合等离子体原子发射光谱仪测定溶液中的镁离子浓度。
5)体外腐蚀速率检测介质的选择
镁合金体外实验的一个重要步骤是选择合适的实验介质。模拟体液组成的不同类型的培养液,有如0.9 wt.% NaCl溶液、SBF、Hanks '溶液、DMEM和PBS溶液。溶液的离子组成和缓冲剂的浓度各不相同。镁合金在不同的溶液中表现出不同的腐蚀响应。
血浆为中性溶液,含有Cl−、HPO4−2、HCO3−、Mg2+、Ca2+,氨基酸、蛋白质、葡萄糖等有机物。下表总结了无机物和有机物含量对可生物降解镁合金腐蚀速率的影响。

表.溶液中无机和有机物含量的影响
注:无机和有机含量对可生物降解镁合金腐蚀速率(CR)的影响(CR中增加↑或减少↓以黑色行表示)。
6)介质溶液的流动速率
体外浸泡试验可在静态或动态状态下进行。大多数研究都是在静态状态下进行的。一些结果表明,静态状态并不代表体内腐蚀。为了更好的模拟体内环境,最好选择动态浸没试验,并且溶液的流速应调整到与植入区域的血液流速相似。
在测试过程中需要特别注意温度控制。与室温相比,体温(37°C)会增加腐蚀速率,并且可以改变腐蚀机制和腐蚀反应的动力学。据报道,在37°C下测得的腐蚀速率比在20°C下测得的高100%以上,即腐蚀速率从室温到37°C增加了两倍。
7)腐蚀疲劳性能
植入物在骨和血管的应用通常是在循环加载条件下,如压缩、拉伸和弯曲之间的变化。疲劳失效发生在循环荷载低于疲劳极限。电化学腐蚀和循环机械载荷的结合导致移植物的腐蚀疲劳,最终导致移植物作用失效。
2 体内腐蚀测量
体外研究中获得的腐蚀结果通常不能如实反映真实的体内腐蚀结果。体液总量影响镁的腐蚀速率,体液量增加会增加镁腐蚀速率,将镁植入小动物体内也并非预测镁合金在人体中的腐蚀过程的合适方法。Witte et al. [2] 通过对镁合金体外和体内的腐蚀速率进行比较,发现在体内的腐蚀速率比在体外的腐蚀速率小约4个数量级,因此优先推荐进行大动物体内实验。
评估体内腐蚀,尤其是硬组织的腐蚀非常困难的。植入物周围的血流量以及氧供应、pH值、腐蚀性介质流量等参数都会影响体内的腐蚀(如髓内植入物比皮下植入物的腐蚀速率更快)。所以如何合理的设计体内模拟实际人体情况的模型就十分重要。
3 腐蚀后的分析以及腐蚀类型
通常在用铬酸溶液清洗镁表面的腐蚀产物前后,在光学显微镜和扫描电子显微镜(SEM)下观察样品的腐蚀形貌。镁合金通常的腐蚀特征是由于微观结构和化学异质性以及合金之间的变化而引起的局部腐蚀。镁的表面形貌在腐蚀过程中发生变化,从微裂纹的形成到腐蚀产物的沉积和生长。
生物可降解镁合金的腐蚀过程包括:1)植入体表面的腐蚀;2)释放出镁离子和其他合金元素;3)大量OH-;4) H2气体。
点蚀和局部腐蚀是镁合金在生理环境下最常见的腐蚀机制,这不仅与合金的非均质结构有关,而且与溶液成分有关。在机械载荷下,不均匀腐蚀的镁合金的机械稳定性可能局部丧失,导致植入物从该部位断裂。
4 组织学研究
动物实验结束后,将植入部位进行组织学研究,以是观察植入物与周围组织的相互作用。通常利用血毒素和伊红染色,可以计算出骨密度和植入体接触面积。可以使用炎症标志物如肿瘤坏死因子α (TNF-α)分析植入物周围的炎症,还可以检测炎症细胞如中性粒细胞、单核细胞、巨噬细胞、多核巨细胞以及破骨细胞数量的增加数量。
▍ 镁基金属在骨科应用的临床试验
通过clinicaltrials数据库检索镁合金正在进行的临床试验[3],有关骨折的注册临床试验有三项,具体内容见下表:
1)The Efficacy and Safety of Magnesium Alloy Screw as a Novel Bioabsorbable Material in Patients Due to Hand Fractures(镁合金螺钉作为一种新型生物可吸收材料在手部骨折患者中的有效性和安全性);NCT02456415
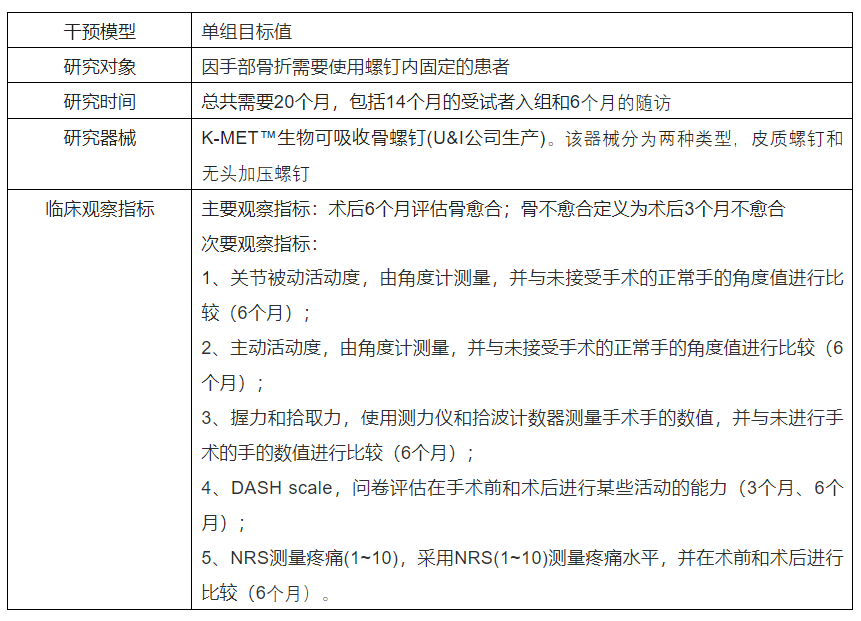
临床试验已经完成,但是并没有发布相关的结果,下表是相关的临床方案的主要内容:
2)Magnesium-based, Bioresorbable Implants for Pediatric Elbow Fractures, a Single Center Pilot Study for Osteosynthesis With Magnezix Screws in Fractures of the Epicondylus Ulnaris and Condylus Radialis(以镁为基础的生物可吸收植入物用于儿童肘关节骨折,一项单中心试点研究用于尺上髁和桡骨髁骨折的螺钉固定)
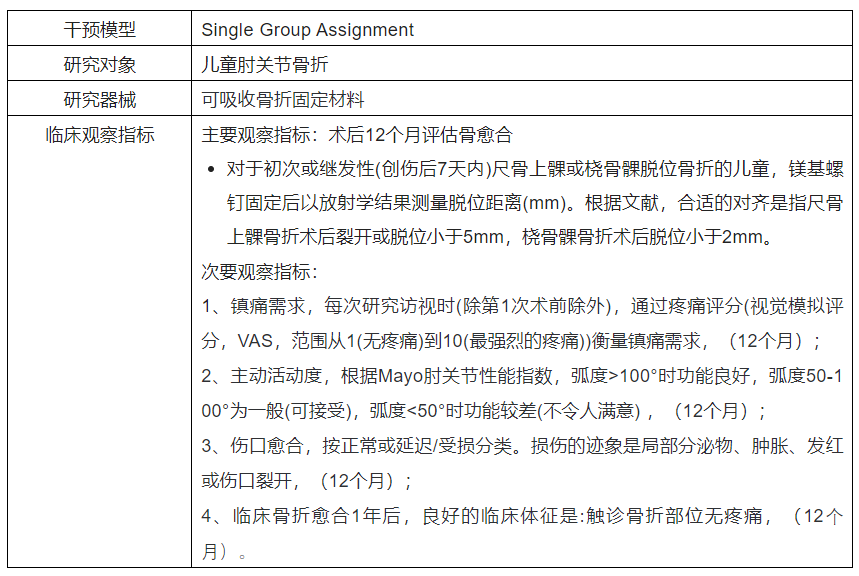
3)Clinical Application of Mg Based Biodegradable Material for Fracture Fixation in the Adult Skeleton(镁基可生物降解材料在成人骨骼骨折固定中的临床应用)

参考资料:
原创声明:欢迎转载,请注明来源和义广业网(heyiguangye.com),否则必究法律责任。
作者声明:感谢本文参考资料作者,文中观点仅供参考,不恰当之处还望包涵指正,资料内容侵删。
作者:杜福崇
审核:晓柏
医疗器械、新材料、人工智能;
一定技术壁垒



