
和义广业【行业研究】之细胞转染行业研究分析,本文详细介绍了细胞转染的概念、转染的类型(如瞬时转染和稳定转染)、转染的技术路线(包括物理法、化学法、生物法及每类方法不同的细分路径),以及国内外代表厂商其转染业务板块中主要的转染试剂产品。本篇主要对细胞转染不同的技术路线中的生物法(腺病毒转染和慢病毒转染)进行梳理分析。
关键词:细胞转染、物理转染、化学转染、生物转染、电穿孔、磷酸钙介导转染、阳离子脂质体转染、聚合物转染、慢病毒转染、腺病毒转染
生物转染法主要指的是病毒介导法,是利用病毒(如腺病毒、慢病毒等)作为载体将外源基因包装后导入细胞,如图所示。病毒本身具有极强的感染性,可用于向相关细胞传递转基因,但是要安全有效地使用病毒作为载体,就必须了解病毒颗粒组合、基因组包装以及导入细胞的目标基因1,将其他基因从病毒基因组中去除,以消除其致病性,然后将转基因与病毒构建体结合后使用了。腺病毒等病毒不会整合到宿主细胞基因组中,而是具有外显表达,因此,其能带来短暂的基因表达;慢病毒可在宿主基因组内整合,从而形成稳定、永久的基因及其产物表达。病毒系统具有高转染效力和治疗基因持续表达的优点,但是,病毒的大规模生产、毒性和插入突变(整合病毒)都有其局限性2。
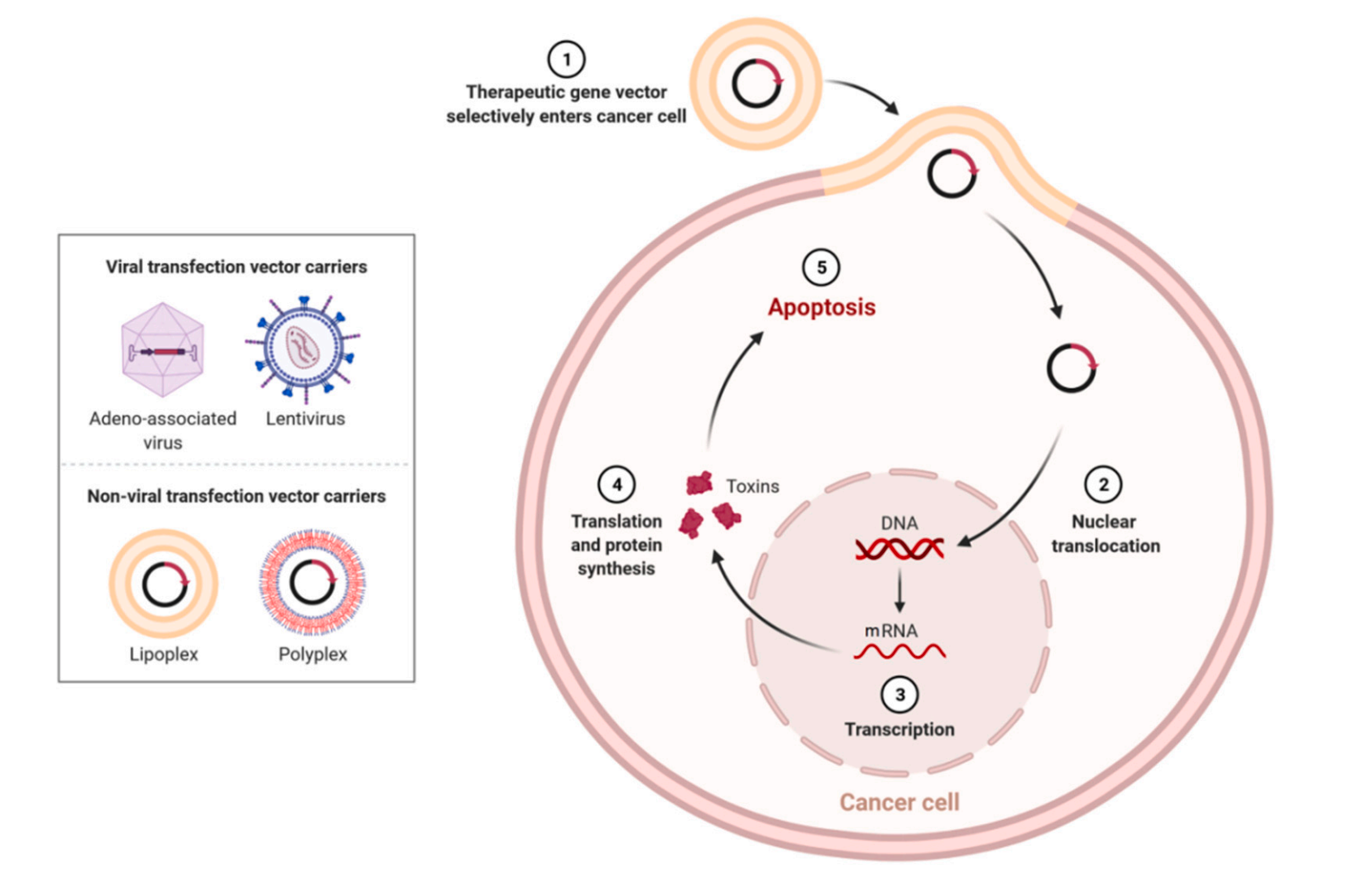
图. 用于癌细胞靶向基因治疗的病毒和非病毒载体
腺病毒(Ads)于1953年首次被发现并从人类腺组织培养物中分离出来。其主要特征:腺病毒是一种特征明确的长度约为 26-40 kb、非整合、无包膜(缺乏外脂层)的线性 dsDNA 病毒,由直径约为 950 Å 的二十面体颗粒覆盖(拉长纤维蛋白除外),分子质量约150 MDa(百万道尔顿)。腺病毒的噬菌体具有病毒趋向性,因此,通过操纵噬菌体可以实现靶向转染3。腺病毒颗粒一般没有脂质或膜,因此在乙醚或乙醇等溶剂中很稳定。最新一代的腺病毒可以传递重达 36 kb 的外来 DNA 片段,由于它们是非整合病毒,即转染后具有外显子表达,因此,基因的表达是短暂的,但在神经元等有丝分裂后的细胞中可以实现长期表达。由于它们不会在宿主基因组中合并,因此排除了插入突变的可能性。但是,腺病毒同样存在一些缺点,如:i) 在适当的腺病毒受体表达量较低的细胞中转染效率较低,需要大剂量的载体才能产生靶细胞细胞毒性;ii) 大剂量的腺病毒往往会产生较高的免疫和炎症反应;iii) 它们通常对化学或物理制剂以及不利的 pH 值条件不稳定,无法在体外长期存活。
腺相关病毒(Adeno-associated viruses ,AAV)是一种包有线性 ssDNA 的小型无包膜病毒,这些病毒对人体无害,是最小的病毒(约22 nm)。在现有的众多 AAV 血清型中,改良 AAV2 被广泛用于基因治疗。这些病毒最初通过与血清特异性细胞表面受体和共受体结合而感染,随后进行内吞,最终逃出内质体,解开外部结构,通过核孔复合体进入细胞核,它们可以整合到 19 号染色体上一个 4 kb 的区域(AAVS1),如下图所示4。
腺相关病毒具有高度稳定,无致病性,不会引发免疫反应等优势,其依靠异源辅助病毒,能更好地控制载体复制过程,使 AAV 载体更安全地应用于基因治疗;AAV 有特定的整合位点,因此发生插入突变的几率很低。普通的 AAV 一般作为外显子实体停留在目标组织内(90%),但也可以与宿主细胞的基因组结合(10%)。然而,转基因的插入大小仅限于 4 kb,很难产生高滴度的病毒。
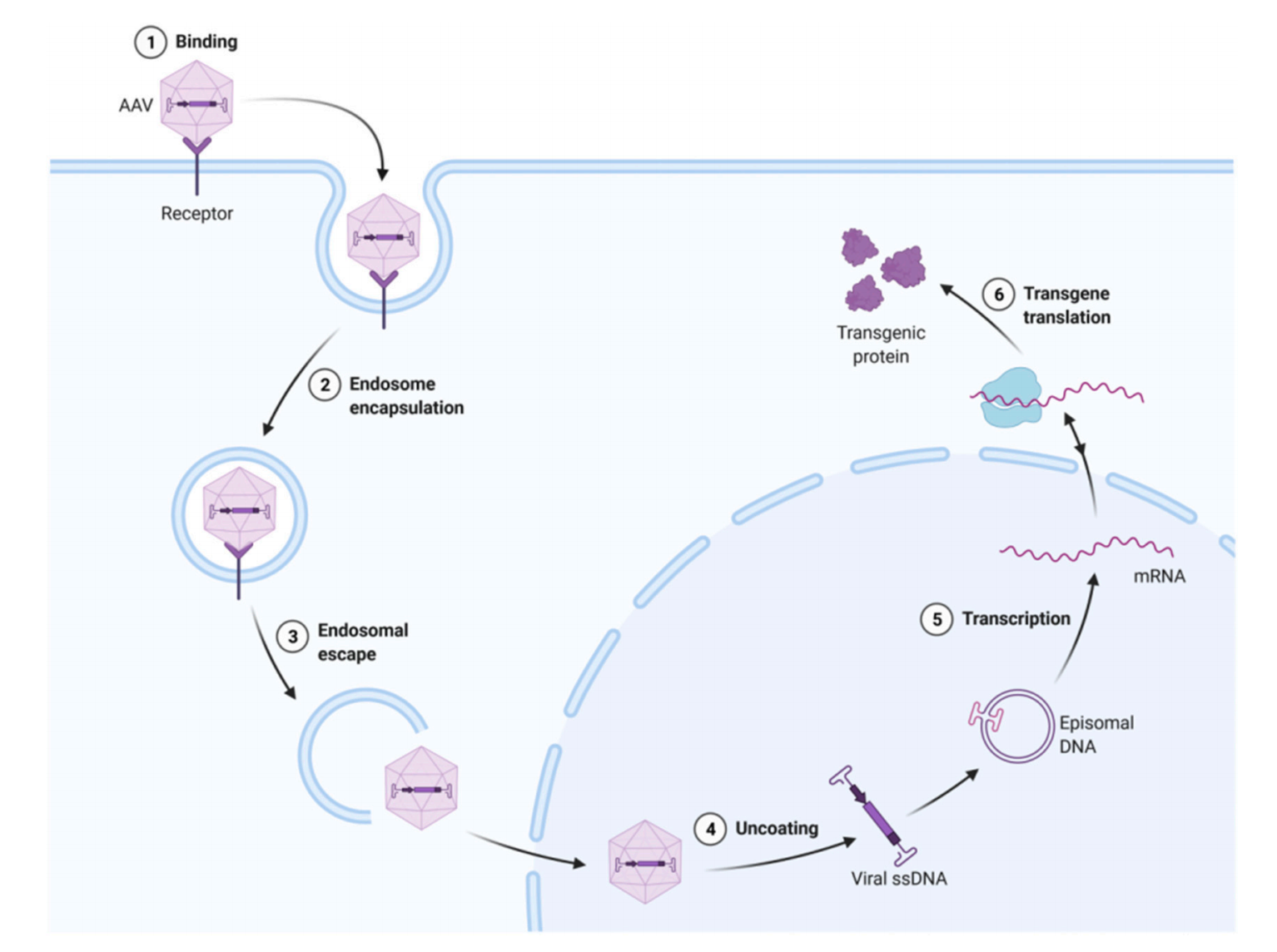
图. AAV 介导的基因治疗
自 20 世纪 90 年代中期以来,作为逆转录病毒亚型的慢病毒已被广泛用作基因递送载体。众所周知,慢病毒可导致潜伏期较长的疾病,其中之一就是人类免疫缺陷病毒(HIV),这些病毒具有在宿主基因组内整合的能力。与其他逆转录病毒属(如也用于基因治疗的γ-逆转录病毒)不同,慢病毒既能影响分裂细胞,也能影响非分裂细胞,这些病毒与目标细胞的核输入系统相互作用,通过核孔控制整合前复合物的主动运输,因此,它们可以将基因转染并传递到非分裂细胞,包括有丝分裂后的细胞(如神经元)和终末分化的细胞(如成纤维细胞)5。
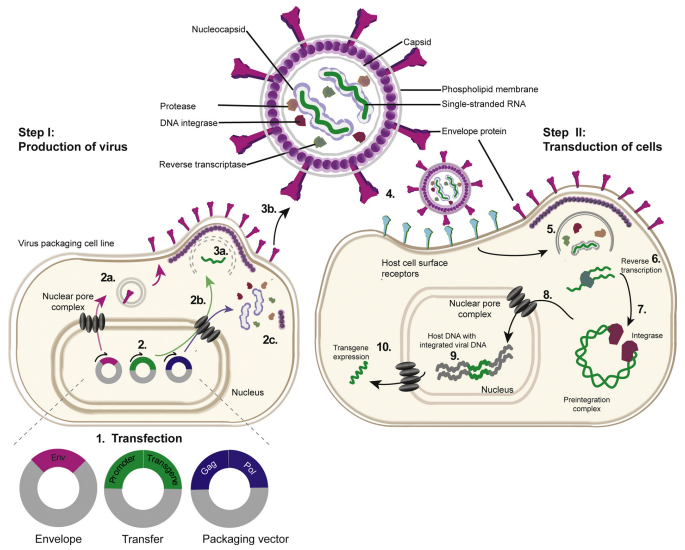
图. 慢病毒转染示意图
与其他逆转录病毒相比,慢病毒有其独特的优点:①较其他逆转录病毒有着更广泛的宿主,对于分裂和非分裂细胞均具有感染能力,对于一些较难转染的细胞,如原代细胞、干细胞、不分化的细胞等,能大大提高目的基因转导效率,使目的基因整合到宿主细胞基因组的几率大大增加。这一特性使得慢病毒载体可以用于采用基因治疗方式治愈疾病的临床试验和研究中,比如一些神经系统方面的疾病;②慢病毒载体携带并整合进入宿主细胞的目的基因对转录沉默作用有一定的抵抗能力,可以在靶细胞中得到持续高效稳定的表达;③慢病毒载体中可以插入组织细胞特异性的启动子和增强子,提高转入基因的转录靶向性,使慢病毒载体中的目的基因在特定的组织细胞中表达;④经过构建后的慢病毒载体可以携带大约5 kb,甚至更长的目的基因,因此除了外源的short-hairpin RNAs(shRNAs)等小分子外,很多cDNA也能被克隆进入慢病毒载体。由于慢病毒载体具有如上众多的优势,使得慢病毒载体成为一种能实现外源基因的高效导入及应用于疾病的基因治疗等多方面的有效工具,具有良好应用前景。
虽然慢病毒载体与其他载体相比具有以上优势,但也有其限制性,主要是生物安全性方面。由于慢病毒载体主要来源为HIV病毒,特别是HIV-1应用的较为广泛和深入,因此慢病毒的生物安全性成为使用者担心的主要问题之一。慢病毒的分子结构被不断改进,主要致力于如何阻止形成有复制能力的HIV病毒,所以我们常用的慢病毒载体中的毒性基因已经被剔除并被外源性目的基因所取代,属于假型病毒。但是由于HIV-1慢病毒载体的自然宿主是人,则病毒仍然具有可能的潜在的生物学危险,建议不要使用编码已知或可能会致癌的基因的假型病毒,除非已经完全公认某个基因肯定没有致癌性,否则均不建议采用假型病毒进行生物学实验6。
小结
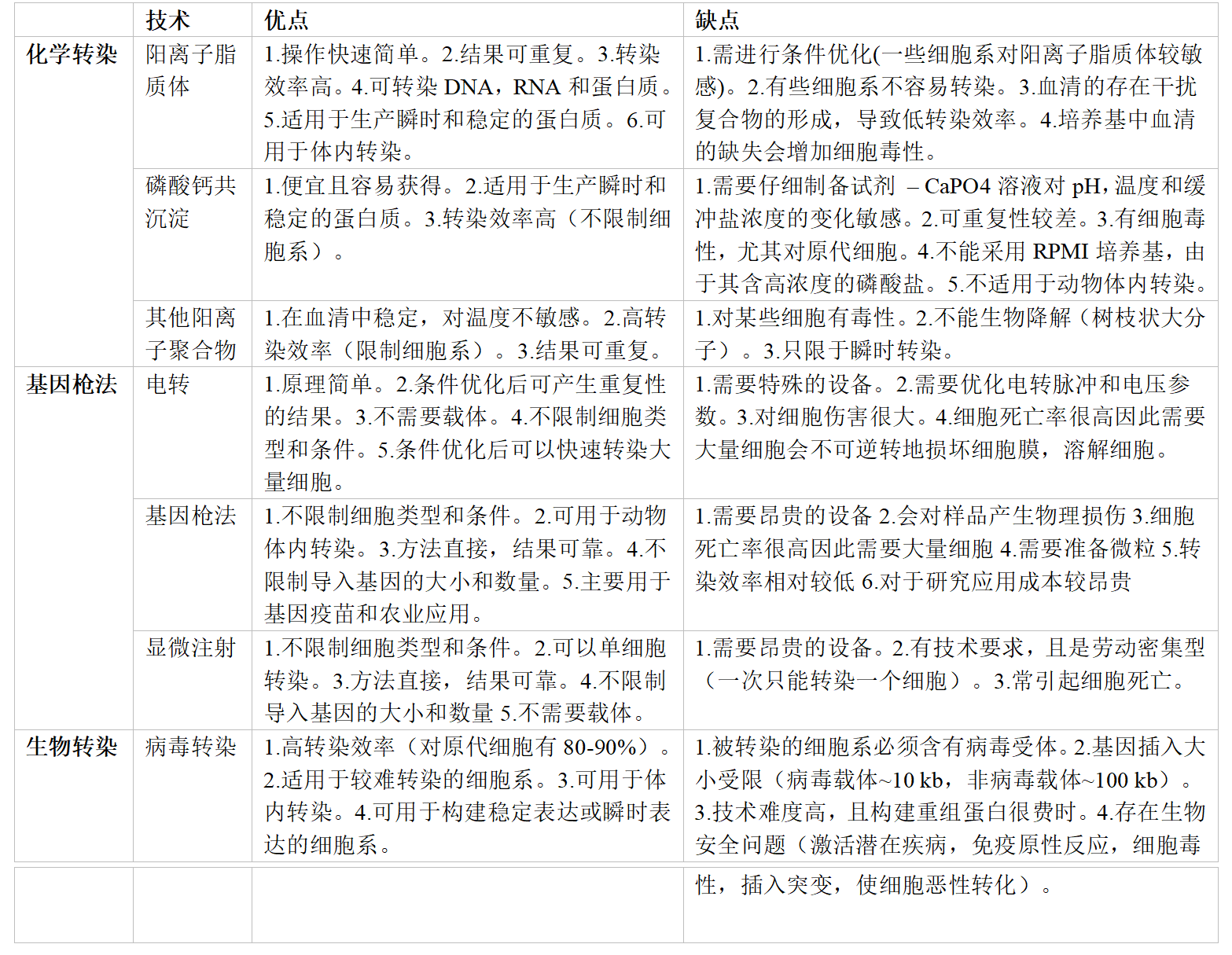
参考文献:
[1]D. Bouard, D. Alazard-Dany, F.L. Cosset, Viral vectors: from virology to transgene expression, Br. J. Pharmacol. 157 (2) (2009) 153–165
[2] M.C. Milone, U. O’Doherty, Clinical use of lentiviral vectors, Leukemia 32 (7) (2018) 1529–1541
[3]J. Kaiser, How safe is a popular gene therapy vector? Science 367 (6474) (2020) 131
[4]Adenovirus: the first effective in vivo gene delivery vector, Hum. Gene Ther. 25 (1) (2014) 3–11.
[5]M.C. Milone, U. O’Doherty, Clinical use of lentiviral vectors, Leukemia 32 (7) (2018) 1529–1541.
[6]Meng F, Chen C, Wan H, Zhou Q. [Advances of lentiviral vectors]. Zhongguo Fei Ai Za Zhi. 2014 Dec; 17(12):870-6. Chinese. doi: 10.3779/j.issn.1009-3419.2014.12.09. PMID: 25539614; PMCID: PMC6000409.
声明:以上根据公开资料整理。如有遗漏,欢迎留言补充。
作者:武瑾嵘
排版:壹 万
医疗器械、新材料、人工智能;
一定技术壁垒



