
和义广业【行业研究】之细胞转染行业研究分析,本文详细介绍了细胞转染的概念、转染的类型(如瞬时转染和稳定转染)、转染的技术路线(包括物理法、化学法、生物法及每类方法不同的细分路径),以及国内外代表厂商其转染业务板块中主要的转染试剂产品。本篇主要对细胞转染不同的技术路线中的物理法(电穿孔技术、显微注射技术、激光辅助转染技术)和化学法(磷酸钙介导的转染、阳离子脂质体转染、阳离子聚合物转染)进行梳理分析。
关键词:细胞转染、物理转染、化学转染、生物转染、电穿孔、磷酸钙介导转染、阳离子脂质体转染、聚合物转染、慢病毒转染、腺病毒转染
将DNA导入至细胞内的方法多种多样,如下图所示,但是没有哪种方法是适合所有情况的,需根据细胞类型和实验需要进行选择,理想的方法应具有高转染效率,低细胞毒性和对正常生理学的影响最小,并且易于使用和可重复性等特点。
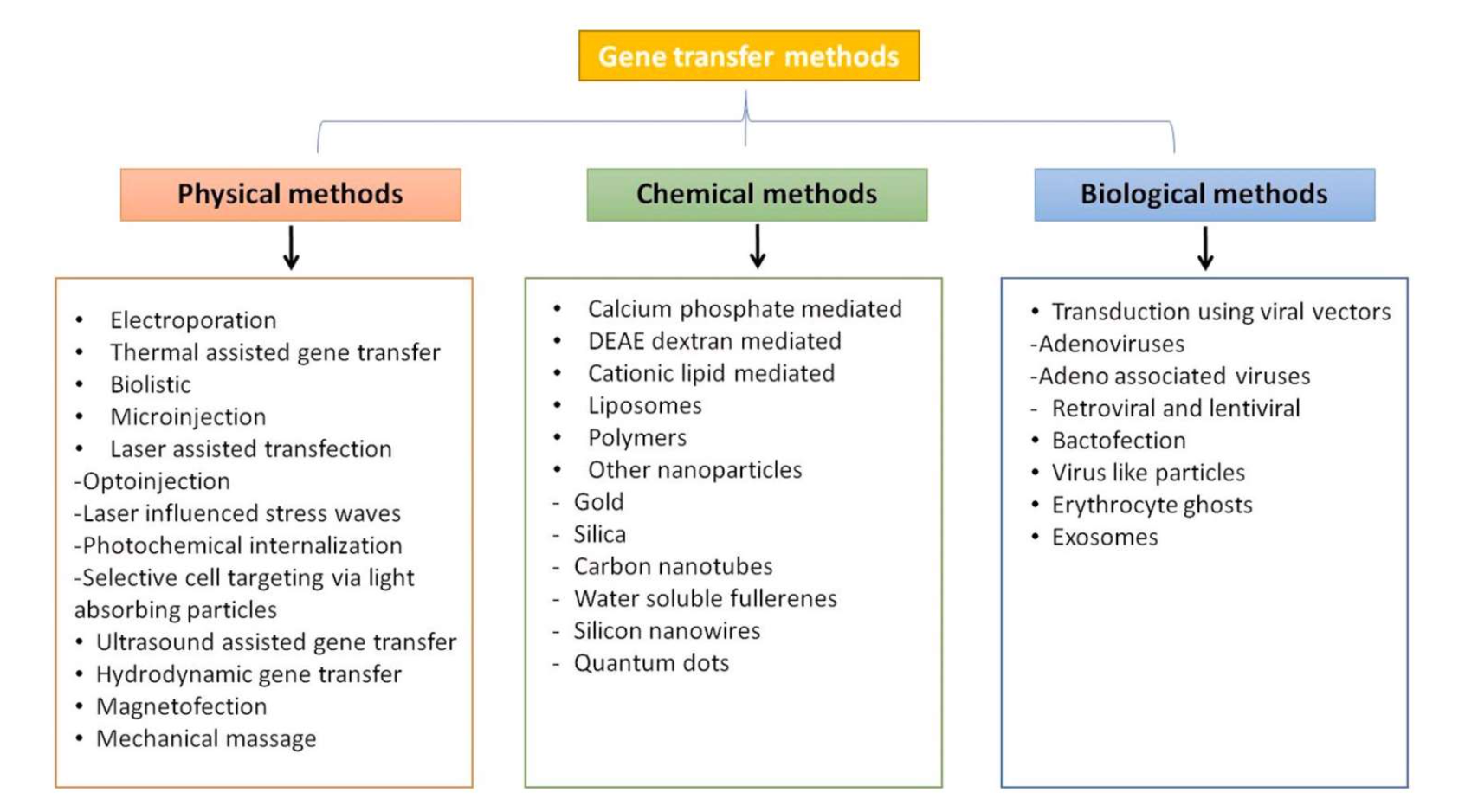
图. 基因转移的方法
物理方法是利用物理强度来提高细胞膜的穿透性,从而帮助传递所需的基因。这种方法的优点是方便可靠。然而,其主要缺点是在此过程中会损伤细胞。这就大大减少了有活力的转染细胞数量。物理方法包括电穿孔法、显微注射法、激光法、高温法、超声波法和流体力学应用法1。
电穿孔是指通过可控的短电脉冲将 DNA 转染到任何细胞中,如下图所示。约 10 ns 的电脉冲足以瞬时改变细胞膜的结构和生理特性,形成半径小于 10 nm 的孔,从而使纳米级寡核苷酸和化合物进入细胞2。此外,电场的存在导致离子通过电泳和电渗进行被动扩散。影响转染效率和细胞活力的因素包括外加电场的强度、宿主细胞暴露于电脉冲的时间、温度、DNA 浓度、DNA 构象和转染介质的离子排列等。电穿孔技术可用于体内和体外基因递送,其优势在于成本低、见效快,与病毒转染一样有效,但是,由于使用这种方法的细胞死亡率很高,因此需要对条件进行大量优化。
目前在体内实施电穿孔的其他挑战有:i) 电场的效率只能在电极周围半径 1 厘米的范围内获得,这使得细胞很难在组织的大范围内转染;ii) 只有通过手术才能将电极植入内脏,这并不可行;iii) 高电压实施时的高温会导致不可修复的组织损伤,也会影响基因组 DNA 的稳定性。
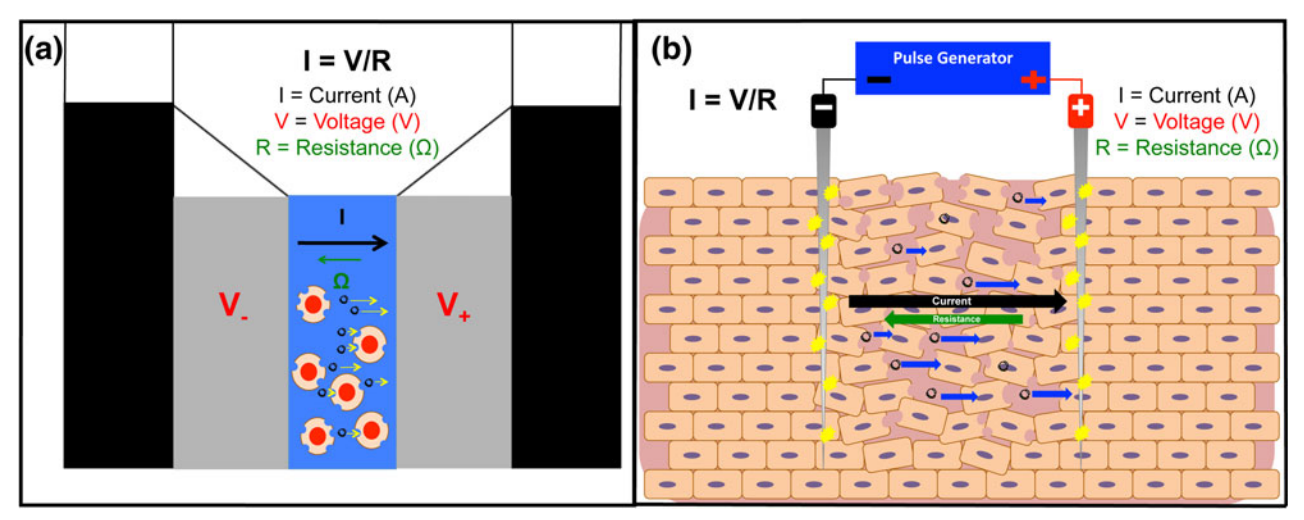
图.电穿孔技术3
显微注射是一种利用微针直接进行基因递送的物理方法,如下图所示。早期的微针由玻璃制成,随着技术的进步,现在可以用硅、金属和生物可降解聚合物制造微针。这些微针可以排列成阵列,并可根据多种给药应用制造。这些微针可以是空心的,内含核酸,也可以是涂有核酸的实心针。微注射递送不仅可用于体外,也可用于体内基因递送,在体外条件下,单个微针已被用于转染小鼠和大鼠卵子,以产生转基因动物,并促进体细胞核移植;在体内条件下,通过皮肤在体内传递核酸,微针可以穿透角质层,然后通过开发微通道在表皮内输送核酸。事实证明,这种方法比电穿孔法更适合通过皮肤引入 DNA 疫苗4。
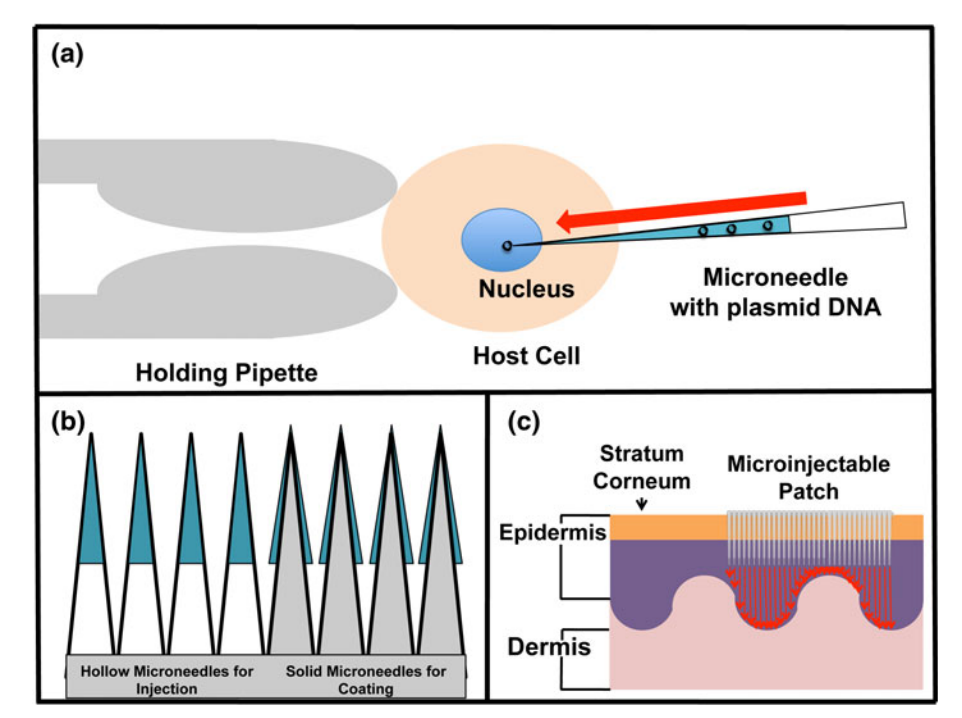
图. 显微注射5
受激发射光放大(Light Amplification by Stimulated Emission of Radiation,LASER)辅助转染也称为光转染、激光转染或光照转染,如下图所示。这一过程的原理是,通过激光脉冲可以瞬时调节细胞膜的通透性,随后形成的孔隙会导致细胞膜和培养基之间的渗透差,从而促进遗传物质和大分子进入所需细胞。激光转染基因递送方法的不同子类型包括:i) 光注射;ii) 激光产生的应力波;iii) 光化学内化;iv) 通过光吸收分子进行特异性靶向6。
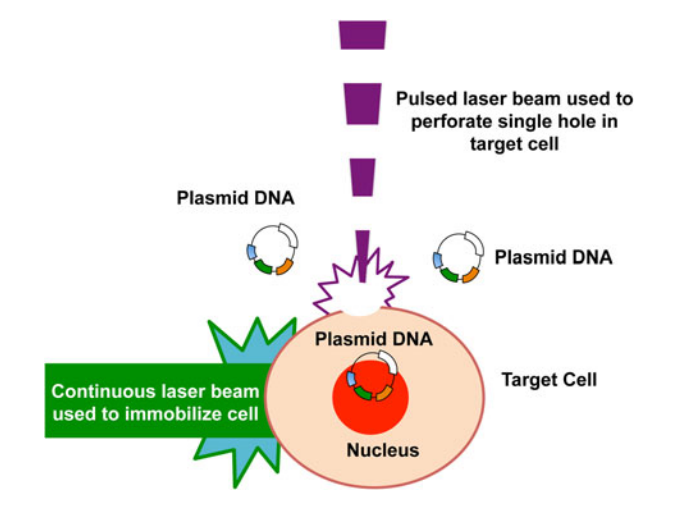
图. 激光辅助转染
化学方法是指利用载体分子包被核酸使其呈现中性电荷或正电荷,如磷酸钙共沉淀法、脂质体转染方法、阳离子聚合物法,如下图所示。
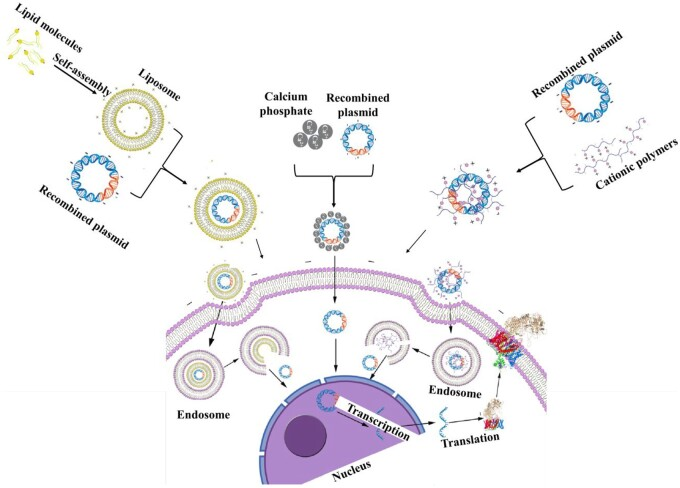
图. 脂质体介导的转染、磷酸钙共沉淀和阳离子聚合物转染方法示意图7
磷酸钙法(Calcium phosphate transfection method):磷酸钙法是一种传统的细胞转染方法,由Graham等于1973年首创,适用于哺乳动物细胞。该方法基于钙离子与DNA结合生成复合物的原理,如下图所示。首先,将外源DNA与钙盐混合,产生钙磷结晶沉淀。然后,将钙磷沉淀与目标细胞一同处理,通常是直接加入到细胞培养基中。转染过程中,细胞通过吞噬作用摄取了外源DNA。该方法简单易行,价格低廉,但转染效率较低,对细胞的毒性较大。
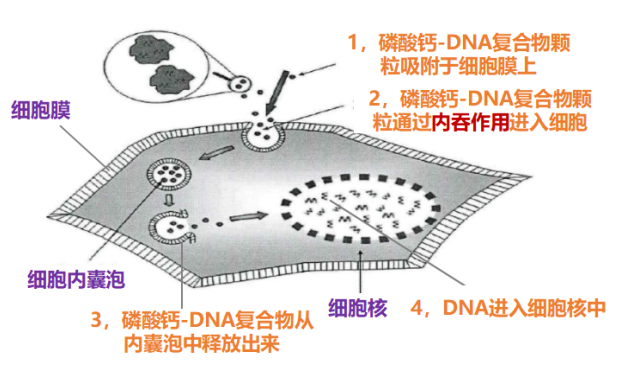
图. 磷酸钙-DNA通过内吞作用进入细胞8
阳离子脂质体法是指脂质体通过表面的正电荷与核酸磷酸基团的负电荷相互作用形成内包DNA分子的复合物,复合物表面带正电,会被带负电的细胞膜所吸附,进而通过融合或细胞内吞完成外源DNA分子的导入,是目前实验室最方便的转染方式之一,如下图所示。
脂质体是一种人工的脂双层膜。可以将DNA包裹到亲水性核心内部,也可将其络合到磷脂片层。1992年,阳离子脂质体首次被用于基因治疗的临床试验。阳离子脂质体通常由阳离子和两性离子脂质组成。在DNA与脂质体形成lipoplex的过程中,阳离子脂质体起到复合和凝集DNA的作用,同时也有助于复合物与细胞膜的结合。大量实验表明阳离子脂质体中的这类组分对细胞的毒性较大,引起了人们的极大关注。此外,由于lipoplex的异质性和不稳定性,阳离子脂质体载体的转染效率明显低于病毒载体。近年来,体内转染研究越来越火热,因阳离子脂质体在血清存在的情况下会迅速失活,无法直接应用于体内研究,这是它的另一个缺点。目前,应用较为广泛的脂质体为Invitrogen Lipofectamine, Dharmacon DharmaFECT系列产品。
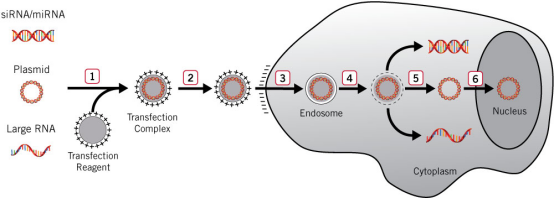
图. 脂质体法转染过程示意图9
阳离子聚合物转染法是指带正电的聚合物与核酸带负电的磷酸基团形成带正电的复合物后与细胞表面带负电的蛋白多糖相互作用,并通过内吞作用进入细胞。阳离子聚合物和阳离子脂质体最大的区别在于阳离子聚合物不含疏水部分而完全溶于水,可以方便地进行化学修饰,且不会像脂质体一样破坏细胞结构,所以相对毒性较低,如下图所示。
目前使用最广泛的阳离子聚合物转染试剂是PEI(聚乙烯亚胺),因其毒性低、成本低、免疫原性低,可将外源基因转染到悬浮细胞或贴壁细胞中。同时,它也是一种适用于瞬时转染人HEK-293T细胞的试剂,尤其适用于大规模生产重组病毒载体。自1995年PEI首次被用于DNA转染以来,就因其安全性和稳定性而被广泛应用于科学研究和基因疗法中。随着PEI技术的不断革新与发展,现在PEI被广泛应用于生命科学研究、非病毒载体体内转染研究、病毒和蛋白生产专用研究中。常见的阳离子聚合物还包括聚氨基酯(PBAE)、壳聚糖(Chitosan)、聚丙烯胺(PAH)、二乙氨乙基葡聚糖(DEAE-dextran)、聚氨树枝状聚合物(PAMAM)等。
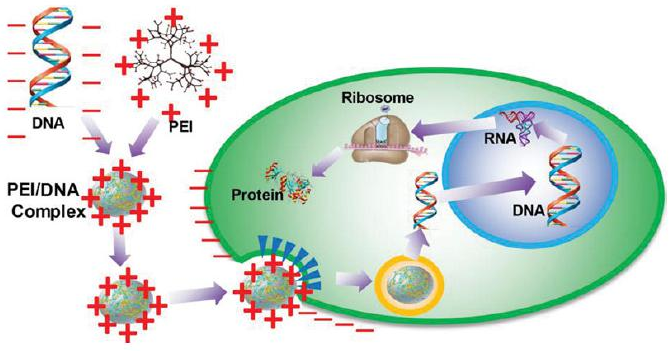
图. 阳离子聚合物转染过程示意图
参考文献:
[1]M. Alsaggar, D. Liu, Chapter one - physical methods for gene transfer, in: L. Huang, D. Liu, E. Wagner (Eds.), Advances in Genetics, Academic Press, 2015, pp. 1–24
[2]J.L. Young, D.A. Dean, Electroporation-mediated gene delivery, Adv. Genet. 89 (2015) 49–88
[3]Mellott AJ, Forrest ML, Detamore MS. Physical non-viral gene delivery methods for tissue engineering. Ann Biomed Eng. 2013 Mar;41(3):446-68. doi: 10.1007/s10439-012-0678-1. Epub 2012 Oct 26. PMID: 23099792; PMCID: PMC5102682.
[4]C.-P. Yao, et al., Laser-based gene transfection and gene therapy, IEEE Trans. Nanobioscience 7 (2) (2008) 111–119.
[5]Yamamoto, F., M. Furusawa, I. Furusawa, and M. Obinata. The ‘pricking’ method. A new efficient technique for mechanically introducing foreign DNA into the nuclei of culture cells. Exp. Cell Res. 142:79–84, 1982.
[6]C.-P. Yao, et al., Laser-based gene transfection and gene therapy, IEEE Trans. Nanobioscience 7 (2) (2008) 111–119.
[7]图片来源:Guo X, Ma Y, Wang H, Yin H, Shi X, Chen Y, Gao G, Sun L, Wang J, Wang Y, Fan D. Status and developmental trends in recombinant collagen preparation technology. Regen Biomater. 2023 Nov 29;11:rbad106. doi: 10.1093/rb/rbad106. PMID: 38173768; PMCID: PMC10761200.
[8]图片来源:网络整理
[9]图片来源:网络整理
声明:以上根据公开资料整理。如有遗漏,欢迎留言补充。
作者:武瑾嵘
排版:壹 万
医疗器械、新材料、人工智能;
一定技术壁垒



